 和-lgc(
和-lgc( )或-
)或- 和-lgc(
和-lgc( )的关系如图所示,下列说法错误的是
)的关系如图所示,下列说法错误的是
A.L2表示- 和-lgc( 和-lgc( )的关系 )的关系 |
| B.H3PO3的电离常数Ka1(H3PO3)的数量级为10-2 |
C.等浓度等体积的H3PO3溶液与NaOH溶液充分混合,c( )<c(H3PO3) )<c(H3PO3) |
D.pH=6.54时,c(Na+ )<3c( ) ) |
 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应
 ,相关数据如下表(已知:炭粉足量)。
,相关数据如下表(已知:炭粉足量)。| 容器 | T/℃ | 物质的起始浓度/( ) ) | 物质的平衡浓度
| ||
 |  |  | |||
| Ⅰ |  | 1.00 | 0 | 0 | 0.85 |
| Ⅱ |  | 0 | 1.00 | 1.00 | x |
| Ⅲ |  | 2.00 | 0 | 0 | 1.60 |
A. | B.达到平衡所需时间: |
C. | D. ℃,该反应的化学平衡常数 ℃,该反应的化学平衡常数 |
 氨水中滴入0.10 mol·
氨水中滴入0.10 mol· 的醋酸,溶液的PH与所加醋酸体积的关系如图所示。下列说法错误的是[已知:
的醋酸,溶液的PH与所加醋酸体积的关系如图所示。下列说法错误的是[已知: ,
, ]
]
A. |
| B.a点的值约为10.85 |
C.b点溶液中, )<0.1 mol · )<0.1 mol · |
D.a,b,c三点溶液中,水的电离度由大到小的顺序为 |


 SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
| A.该反应为放热反应,v正,a<v逆,b |
| B.T1 K时平衡体系中可通过移走SiCl4提高SiHCl3的转化率 |
| C.当反应进行到a处时,v正/v逆=16/9 |
| D.T2 K时平衡体系中再充入1 mol SiHCl3,平衡正向移动,x(SiH2Cl2)增大 |
 的物质的量为bV mol
的物质的量为bV mol mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为 L
L mol
mol| A.①②③④⑤ | B.①③④⑤ |
| C.①③⑤ | D.①②③⑤ |
 、
、 ,含少量
,含少量 和
和 )为原料先制备硫酸铜,再由硫酸铜制备碱式碳酸铜[
)为原料先制备硫酸铜,再由硫酸铜制备碱式碳酸铜[ ]。实验包括如下过程:
]。实验包括如下过程: ,过滤。
,过滤。
 所发生反应的离子方程式:
所发生反应的离子方程式: 的目的是
的目的是 ]
] 。
。 溶液调节
溶液调节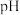 范围为
范围为 溶液。{设
溶液。{设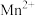 、
、 开始沉淀时
开始沉淀时 ,沉淀完全时
,沉淀完全时 。
。 ,
, }
} 。
。 的产率{
的产率{ }随起始
}随起始 与
与 的比值和溶液pH的关系如图2所示。
的比值和溶液pH的关系如图2所示。
 的实验方案:向烧杯中加入
的实验方案:向烧杯中加入 溶液,将烧杯置于70℃的水浴中,
溶液,将烧杯置于70℃的水浴中, 。(实验中可选用的试剂或仪器:
。(实验中可选用的试剂或仪器: 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 盐酸、pH计)
盐酸、pH计) 的产率偏低,但Cu元素含量偏大,原因是
的产率偏低,但Cu元素含量偏大,原因是 )为原料进行生产并综合利用的某过程如下图所示。已知:Ksp[Mg(OH)2]=5.6×10-12;Ksp[CaMg(CO3)2]<< Ksp[Mg(OH)2]。
)为原料进行生产并综合利用的某过程如下图所示。已知:Ksp[Mg(OH)2]=5.6×10-12;Ksp[CaMg(CO3)2]<< Ksp[Mg(OH)2]。

 NC13十3H2↑。
NC13十3H2↑。
 和
和 的混合物中加入某浓度的稀硝酸
的混合物中加入某浓度的稀硝酸 ,固体物质完全反应,得到标准状况下
,固体物质完全反应,得到标准状况下 和
和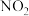 的混合气体及
的混合气体及 。在所得溶液中加入
。在所得溶液中加入 的NaOH溶液
的NaOH溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列有关说法正确的是
。下列有关说法正确的是 与
与 的物质的量之比为
的物质的量之比为

 、
、 与硝酸反应后剩余
与硝酸反应后剩余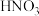 为
为
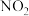 的体积为
的体积为

| A.①⑤ | B.②④ | C.①④ | D.②③ |
| A.11.2 L | B.6.72 L | C.8.96 L | D.4.48 L |