铁及其化合物在日常生活、工业生产中均发挥着重要的作用。
铁是人体中不可或缺的微量元素
(1)正常情况下,从食物中获取的铁就能满足人体对铁的需要。菠菜中的铁元素以草酸亚铁(FeC
2O
4,淡黄色难溶于水的晶体)的形式存在。FeC
2O
4常用于照相显影剂和制药工业,常温下性质稳定,受热会生成三种常见的氧化物:Fe
2+、

都能使酸性高锰酸钾溶液褪色。为了验证菠菜中Fe
2+的存在,小明同学设计了如下实验:
①预处理:灼烧菠菜,可能发生的化学反应是
___________ (用化学方程式表示)。
②酸浸:用硫酸浸泡,在浸泡时,加入足量
___________脱色用于排除菠菜本身的颜色干扰。
③过滤:除去不溶物。
④检验:在滤液中加入酸性高锰酸钾溶液,若观察到
___________,则菠菜中确实存在Fe
2+。
(2)琥珀酸亚铁片是一种常见的补血剂,其说明书如图所示:
名称:琥珀酸亚铁口服片
主要成分的化学式:C4H4FeO4
含量:每片含琥珀酸亚铁0.1g
适应症:用于治疗缺铁性血治疗
用量:成人一日2—4片
儿童一日1—3片,分次服用 |
琥珀酸亚铁口服片说明书
①片剂表面通常包裹着用淀粉制作的糖衣,淀粉属于
___________(填“无机物”或“有机物”),糖衣除了改善药物口感外,另一个作用是
___________。
②根据说明书计算,成人每天最多可补充铁元素质量为
___________g(保留小数点后两位)。
铁是工业上一种用途广泛的金属材料
(3)铁红(主要成分Fe
2O
3)是一种红棕色粉末,用于油漆、油墨、橡胶等工业中,用工业废料铁尾渣制备高品质铁红的方法,为铁红涂料的制备提供了新途径。

①下列说法正确的是
___________。
a.“酸溶”时,将铁尾渣加水调浆、升温至85—90℃,均有利于加快反应速率
b.加氨水调节pH时,将温度冷却至15℃,是为了减缓化学反应速率
c.催化剂仅能改变化学反应速率,对产率无影响
②根据下列信息,在还原步骤时,应选用较合适的还原剂种类和温度分别是
___________。

③在氧化步骤中发生的反应主要是:

,最后获得的Fe
2O
3固体需进行洗涤,判断洗净的方法是:取最后一次洗涤液,
___________。




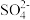 ,其个数之比为1:6:5,含铜离子0.64%。为了除去重金属铜离子,处理100吨该工厂废水需要加入生石灰固体较合理的质量为
,其个数之比为1:6:5,含铜离子0.64%。为了除去重金属铜离子,处理100吨该工厂废水需要加入生石灰固体较合理的质量为


 ;
; 都能使酸性高锰酸钾溶液褪色。为了验证菠菜中Fe2+的存在,小明同学设计了如下实验:
都能使酸性高锰酸钾溶液褪色。为了验证菠菜中Fe2+的存在,小明同学设计了如下实验:

 ,最后获得的Fe2O3固体需进行洗涤,判断洗净的方法是:取最后一次洗涤液,
,最后获得的Fe2O3固体需进行洗涤,判断洗净的方法是:取最后一次洗涤液,
 ”图,图中“一”两端的物质相互能反应。下列说法不正确的是
”图,图中“一”两端的物质相互能反应。下列说法不正确的是


 某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示,则t1时刻,KMnO4开始分解
某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示,则t1时刻,KMnO4开始分解 在一定量硝酸银和硝酸铜的混合溶液中加入铁粉,充分反应,硝酸根质量分数随加入铁粉质量变化如图所示
在一定量硝酸银和硝酸铜的混合溶液中加入铁粉,充分反应,硝酸根质量分数随加入铁粉质量变化如图所示 密闭容器中发生化学反应,X、Y、Z的质量随着反应时间的变化如图所示,则该反应的化学方程式一定为3X+Y=4Z
密闭容器中发生化学反应,X、Y、Z的质量随着反应时间的变化如图所示,则该反应的化学方程式一定为3X+Y=4Z 稀硫酸和氢氧化钠溶液反应的pH的变化图象如图所示,图中c点时,可以加BaCl2溶液来检验硫酸是否被反应完
稀硫酸和氢氧化钠溶液反应的pH的变化图象如图所示,图中c点时,可以加BaCl2溶液来检验硫酸是否被反应完 在稀盐酸中加入氯化镁,然后向其中逐滴加入NaOH溶液
在稀盐酸中加入氯化镁,然后向其中逐滴加入NaOH溶液 在NaOH溶液中加入CaCO3,然后向其中逐滴加入稀盐酸
在NaOH溶液中加入CaCO3,然后向其中逐滴加入稀盐酸 在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸
在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸 在NaOH溶液中加入Ba(NO3)2,然后向其中逐滴加入稀硫酸
在NaOH溶液中加入Ba(NO3)2,然后向其中逐滴加入稀硫酸