
 互为等电子体的分子有
互为等电子体的分子有 的沸点低于
的沸点低于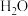 ,其原因是
,其原因是
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为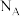 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。 
 为燃料模拟研究该过程。
为燃料模拟研究该过程。 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。 随温度升高而增大的原因是
随温度升高而增大的原因是 ℃以下,原因是
℃以下,原因是 为21%]
为21%]
 和8mol
和8mol ,维持温度为
,维持温度为 ℃,发生反应:
℃,发生反应: 。反应起始时压强为
。反应起始时压强为 ,达到平衡状态时,容器内气体压强是起始压强的2.0倍。平衡时,
,达到平衡状态时,容器内气体压强是起始压强的2.0倍。平衡时, 与
与 物质的量浓度之比
物质的量浓度之比

 的代数式表示,分压=总压×物质的量分数)。
的代数式表示,分压=总压×物质的量分数)。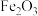 载氧体样品的影响,如图所示。已知:
载氧体样品的影响,如图所示。已知: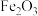 在还原过程中按
在还原过程中按 逐级转变。
逐级转变。
 、
、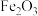 、
、 、
、 )中回收钪,同时生产聚合氯化铁铝[
)中回收钪,同时生产聚合氯化铁铝[ ]具有极其重要的工业价值,一种工艺流程如图所示:
]具有极其重要的工业价值,一种工艺流程如图所示:
 。请回答以下问题:
。请回答以下问题: 沉淀会溶解。写出
沉淀会溶解。写出 与过量NaOH溶液反应生成
与过量NaOH溶液反应生成 的含钪产物的离子方程式:
的含钪产物的离子方程式: 形成的措施有
形成的措施有 ]的化学方程式为
]的化学方程式为 存在时,三价Sc的存在形式与
存在时,三价Sc的存在形式与 、pH的关系如图所示。请判断当
、pH的关系如图所示。请判断当 ,
, 时三价Sc的存在形式为
时三价Sc的存在形式为 )。
)。
 将
将 转化为草酸钪沉淀。向含
转化为草酸钪沉淀。向含 溶液中加入一定量
溶液中加入一定量 溶液,调节溶液的
溶液,调节溶液的 ,当
,当 浓度为
浓度为 -时,
-时, 开始沉淀,则
开始沉淀,则
 的
的 ,
, ;
; (用含a、c、
(用含a、c、 、
、 和
和 的计算式表示)
的计算式表示) 
| A.曲线③表示H2NCH2COO- |
| B.甘氨酸溶液显弱酸性 |
| C.pH=7时,c(H3N+CH2COO-)>c(H2NCH2COO-)>c(H3N+CH2COOH) |
| D.H2NCH2COONa溶液中c(OH-)=c(H3N+CH2COO-)+c(H+) |


| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 80 | 74.2 | 69.2 | 65.2 | 61.6 | 57.6 | 57.6 |
 ,则前120min内平均反应速率v(CH2ClCHClCH3)=
,则前120min内平均反应速率v(CH2ClCHClCH3)= 和Au如反应可以得到一种化合物A,将A缓慢加热到60℃可得到一橙红色的金的氟化物B,经化学分析,A的化学成分为Kr:20.25%、Au:47.60%,F:32.14%;B中含Au 67.47%,含F 32.53%。
和Au如反应可以得到一种化合物A,将A缓慢加热到60℃可得到一橙红色的金的氟化物B,经化学分析,A的化学成分为Kr:20.25%、Au:47.60%,F:32.14%;B中含Au 67.47%,含F 32.53%。 与Au反应制取化合物A的化学方程式为
与Au反应制取化合物A的化学方程式为 在0℃时测得该溶液的核磁共振谱,表明二氟化氪的两个氟原子是等同的,据此说明
在0℃时测得该溶液的核磁共振谱,表明二氟化氪的两个氟原子是等同的,据此说明 在HF中的存在形式
在HF中的存在形式 是唯一通过吸热反应而生成的,这一点具有什么潜在意义?
是唯一通过吸热反应而生成的,这一点具有什么潜在意义?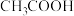 溶液为例),在直流电场作用下,双极膜间的水解离成
溶液为例),在直流电场作用下,双极膜间的水解离成 和
和 。下列说法正确的是
。下列说法正确的是
| A.膜a为阴离子交换膜,膜b为阳离子交换膜 |
| B.产品室生成的物质为盐酸 |
| C.当阴极产生22.4L气体时,理论上可除去模拟海水中11.7g NaCl |
D.阳极反应式为: |
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 9.0 | 4.8 | 0 | 0 |
NO体积/ | 1120 | 2240 | 3360 | V |
A.表中 | B.硝酸的浓度为 |
C.原混合物总质量为 | D.混合物中Fe和Cu的物质的量之比为1∶1 |
 C2H4(g) + 4H2O(g) ΔH。CO2的平衡转化率
C2H4(g) + 4H2O(g) ΔH。CO2的平衡转化率
| A.该反应的ΔH > 0 |
| B.氢碳比:X< 2.0 |
| C.在氢碳比为2.0时,Q点v(逆)小于P点的v(逆) |
| D.P点温度下,反应的平衡常数为512 |


 ,则X晶体的密度为
,则X晶体的密度为