 )是制备硅烷、多晶硅的重要原料。已知
)是制备硅烷、多晶硅的重要原料。已知 在催化剂作用下发生反应:
在催化剂作用下发生反应: 。一定条件下,向容积为1L的恒容密闭容器中充入
。一定条件下,向容积为1L的恒容密闭容器中充入 ,分别在温度为
,分别在温度为 、
、 条件下反应,测得反应体系中
条件下反应,测得反应体系中 的物质的量分数随时间变化的关系如图所示:
的物质的量分数随时间变化的关系如图所示:
 温度下,
温度下, 的平衡转化率
的平衡转化率
 的平衡转化率,除改变温度外还可以采取的措施是
的平衡转化率,除改变温度外还可以采取的措施是A. | B.混合气体的密度不再发生变化 |
C. 与 与 的浓度之比不再改变 的浓度之比不再改变 | D.混合气体的平均摩尔质量不再发生变化 |
 ,
, 、
、 分别表示正、逆反应速率常数,
分别表示正、逆反应速率常数, 为组分B的物质的量分数。
为组分B的物质的量分数。

 配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为188g/mol,则M元素为
配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为188g/mol,则M元素为
 )可帮助植物解除重金属中毒。W、X、Y、Z为原子序数依次增大的前20号元素。该化合物的热重曲线如图所示下列说法错误的是
)可帮助植物解除重金属中毒。W、X、Y、Z为原子序数依次增大的前20号元素。该化合物的热重曲线如图所示下列说法错误的是
| A.W、X、Y能形成多种酸 | B.原子半径: |
C. 左右热分解会产生有毒气体 左右热分解会产生有毒气体 | D. 热分解后生成固体化合物是ZY 热分解后生成固体化合物是ZY |
 的晶体空隙中插入金属离子可获得超导体。一种超导体的面心立方晶胞如图1所示,已知:晶胞参数为
的晶体空隙中插入金属离子可获得超导体。一种超导体的面心立方晶胞如图1所示,已知:晶胞参数为 ,各点的原子分数坐标分别为
,各点的原子分数坐标分别为 ,
, 。下列说法错误的是
。下列说法错误的是
| A.通过A原子的对角面结构如图2所示 | B.相邻两个 的最短距离为 的最短距离为 |
C.晶胞中C点原子分数坐标为 | D.该晶体的密度表达式为 |
 。写出
。写出 与
与 在液氨中发生中和反应的化学方程式为
在液氨中发生中和反应的化学方程式为 ,恒压密闭容器中,起始时
,恒压密闭容器中,起始时 ,不同温度(T)下平衡混合物中
,不同温度(T)下平衡混合物中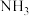 物质的量分数随压强的变化曲线如图所示。
物质的量分数随压强的变化曲线如图所示。
 和
和 的燃烧热
的燃烧热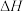 分别为akJ/mol和bkJ/mol,上述合成氨反应的焓变为
分别为akJ/mol和bkJ/mol,上述合成氨反应的焓变为 变为
变为 ,则此时浓度商Q
,则此时浓度商Q )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。 ,式中k(逆)为逆反应的速率常数(只与温度有关)。从C点开始减小压强,平衡发生移动,直至达到新的平衡,v(逆)的变化过程为
,式中k(逆)为逆反应的速率常数(只与温度有关)。从C点开始减小压强,平衡发生移动,直至达到新的平衡,v(逆)的变化过程为
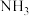 的电极反应式为
的电极反应式为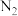 与
与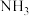 的物质的量之比为
的物质的量之比为 )
)  )的性质与氨相似。25℃时,实验室里用0.1mol/L的盐酸溶液滴定20mL0.1mol/L甲胺溶液,滴定曲线如图所示。(已知:
)的性质与氨相似。25℃时,实验室里用0.1mol/L的盐酸溶液滴定20mL0.1mol/L甲胺溶液,滴定曲线如图所示。(已知: )下列说法不正确的是
)下列说法不正确的是
| A.该滴定过程应该选择甲基橙作为指示剂 |
| B.水的电离程度:c>d |
C. |
D.b点溶液中存在: |
 有多种结构变体,气态时主要以单分子存在,固态时分子有三种变体,其中
有多种结构变体,气态时主要以单分子存在,固态时分子有三种变体,其中 和
和 分子结构如图所示,下列说法错误的是
分子结构如图所示,下列说法错误的是
A.气态 分子构型为平面三角形 分子构型为平面三角形 |
B. 中a对应的键长比b对应的键长短 中a对应的键长比b对应的键长短 |
C. 和 和 中硫原子均采取 中硫原子均采取 杂化 杂化 |
D. 形成的固体中作用力只有共价键 形成的固体中作用力只有共价键 |
 常常作为有机反应的催化剂,画出基态
常常作为有机反应的催化剂,画出基态 原子的价层电子轨道表示式
原子的价层电子轨道表示式 可先制得
可先制得 ,其中C原子的杂化方式为
,其中C原子的杂化方式为 具有优良的还原性,易被氧化成
具有优良的还原性,易被氧化成 。测得乙二酸中的
。测得乙二酸中的 的键长比普通
的键长比普通 的键长要长,说明理由
的键长要长,说明理由
| A.现代化学,常利用原子光谱上特征谱线鉴定元素 |
| B.电负性大于1.8一定是非金属 |
| C.配合物的稳定性不仅与配体有关,还与中心原子的所带电荷等因素有关。 |
D. 晶体的密度为 晶体的密度为 ,图示晶胞 ,图示晶胞 与 与 的距离 的距离 |


 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和四面体。电池充放电时,
的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和四面体。电池充放电时, 脱出或嵌入
脱出或嵌入 形成结构示意图如(b)所示。下列说法正确的是
形成结构示意图如(b)所示。下列说法正确的是
A.每个 晶胞中 晶胞中 个数为1-x 个数为1-x |
| B.图(b)中x=0.1875 |
C.图(b)中 |
D.当 转化为 转化为 时,每转移电子 时,每转移电子 ,嵌入 ,嵌入  |
 加氢是制取乙醇的主要反应。反应如下:
加氢是制取乙醇的主要反应。反应如下:



A. | B.容器中气体的平均摩尔质量不再变化 |
| C.混合气体的密度不再变化 | D. 不再变化 不再变化 |
 的关系如图1所示。氢酯比在2~9之间,乙醇的选择性随氢酯比增大而逐渐增大的原因为
的关系如图1所示。氢酯比在2~9之间,乙醇的选择性随氢酯比增大而逐渐增大的原因为
 的恒压密闭容器中,通入
的恒压密闭容器中,通入 和
和 发生反应I和II,测得不同温度下达平衡时
发生反应I和II,测得不同温度下达平衡时 转化率和乙醇的选择性如图2所示。260℃时反应I的标准平衡常数为
转化率和乙醇的选择性如图2所示。260℃时反应I的标准平衡常数为
 ,其标准平衡常数:
,其标准平衡常数: 。温度高于240℃时,随温度升高乙酸甲酯的转化率降低的原因是
。温度高于240℃时,随温度升高乙酸甲酯的转化率降低的原因是 ]
]
 (
( 为活化能-假设受温度影响忽略不计,
为活化能-假设受温度影响忽略不计, 为速率常数,R和C为常数),为探究催化剂
为速率常数,R和C为常数),为探究催化剂 、
、 的催化效率,进行了相应的实验,依据实验数据获得图3曲线。假设催化剂
的催化效率,进行了相应的实验,依据实验数据获得图3曲线。假设催化剂 的催化效率大于
的催化效率大于 的催化效率,请在图3中画出催化剂
的催化效率,请在图3中画出催化剂 的相应图线并标注
的相应图线并标注
 过程中可能发生下列反应。
过程中可能发生下列反应。






 平衡常数K将
平衡常数K将
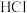 与1
与1
 制氯乙烯(
制氯乙烯( ),在1L刚性容器中反应3h,实验数据如下图。
),在1L刚性容器中反应3h,实验数据如下图。


 作用下上述反应的反应历程如图所示。“2→3”的化学方程式可表示为:
作用下上述反应的反应历程如图所示。“2→3”的化学方程式可表示为:

 分压不变,
分压不变,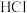 分压过高时反应催化效率降低的可能原因是
分压过高时反应催化效率降低的可能原因是 还原为
还原为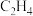 ,其原理示意图如下:
,其原理示意图如下:
 ,出口处气体的总体积为进口处的x倍,则
,出口处气体的总体积为进口处的x倍,则 转化率为
转化率为