 由三种元素组成。某学习小组开展如下探究实验:
由三种元素组成。某学习小组开展如下探究实验:
 的元素有
的元素有 的化学式为
的化学式为 和加热一定的温度下制得,请写出相应的方程式
和加热一定的温度下制得,请写出相应的方程式 能溶于
能溶于 的水溶液,产物中含一种正八面体的负三价阴离子,写出其相应的离子方程式
的水溶液,产物中含一种正八面体的负三价阴离子,写出其相应的离子方程式 ,其中n代表大π键的原子数,m代表大π键的电子数,下列说法正确的是
,其中n代表大π键的原子数,m代表大π键的电子数,下列说法正确的是| A.在氧族气态氢化物中,H2Se的沸点最低 | B.SeO 和SeO3的空间结构相同 和SeO3的空间结构相同 |
C.SO 中的键角小于SO3中的键角 中的键角小于SO3中的键角 | D.噻吩( )含有的大π键为π )含有的大π键为π |
 )为原料进行“加碳氯化”的方法生产
)为原料进行“加碳氯化”的方法生产 ,相应的化学方程式为:
,相应的化学方程式为:

 的平衡转化率的是
的平衡转化率的是 的含量
的含量 下
下 可直接分解制取
可直接分解制取 ,反应的原理如下:
,反应的原理如下: 。实际生产中往刚性容器中同时通入
。实际生产中往刚性容器中同时通入 和水蒸气,水蒸气与反应体系的任何物质均不发生反应,测得容器总压总压)和
和水蒸气,水蒸气与反应体系的任何物质均不发生反应,测得容器总压总压)和 的转化率(a)随时间的变化关系如图1所示。计算反应在
的转化率(a)随时间的变化关系如图1所示。计算反应在 内的平均反应速率
内的平均反应速率
 ;平衡时,平衡常数
;平衡时,平衡常数
 (
( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
 的反应历程分两步:
的反应历程分两步:

 浓度,反应速率将
浓度,反应速率将 浓度反应速率
浓度反应速率
 ,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:
,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:


 有利于提高氧化效果,原因是
有利于提高氧化效果,原因是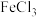 和
和 溶液在乙醇和水的混合溶液中混合搅拌(
溶液在乙醇和水的混合溶液中混合搅拌(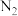 氛围),充分反应得到纳米零价铁、
氛围),充分反应得到纳米零价铁、 、HCl、NaCl和
、HCl、NaCl和 。写出反应的化学方程式
。写出反应的化学方程式

 的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是
的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是

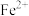 氧化为
氧化为 ,控制pH可形成
,控制pH可形成 沉淀。写出该反应的离子方程式:
沉淀。写出该反应的离子方程式: 转化为
转化为 沉淀除去。若溶液pH偏低,将会导致
沉淀除去。若溶液pH偏低,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是 、
、 ]。
]。
 )相比,芳香基磷酸酯更适合高酸度废水中
)相比,芳香基磷酸酯更适合高酸度废水中 的萃取,原因是
的萃取,原因是 、
、 、
、 溶液)为原料,制备
溶液)为原料,制备 的实验方案:
的实验方案: 、
、 的萃取率-pH的关系曲线如图所示。实验中须使用的试剂有:Cyanex272、
的萃取率-pH的关系曲线如图所示。实验中须使用的试剂有:Cyanex272、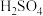 溶液、NaOH溶液)。
溶液、NaOH溶液)。
 铂、铬
铂、铬 等金属及其化合物在工业上有重要用途,
等金属及其化合物在工业上有重要用途, 与
与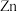 位于同一副族,且在
位于同一副族,且在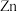 的下一周期。
的下一周期。A. | B. | C. | D. |
 和
和 中,分解温度较高的是
中,分解温度较高的是 熔点为
熔点为 ,
, 熔点为
熔点为 ,
, 熔点更高的原因是
熔点更高的原因是 原子的两种杂化方式为
原子的两种杂化方式为 的价态为
的价态为
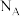 代表阿伏加德罗常数的值,则该晶体的密度为
代表阿伏加德罗常数的值,则该晶体的密度为 。其中
。其中 的阴离子配位数为
的阴离子配位数为
 为原料,通过下列合成路线合成有机物
为原料,通过下列合成路线合成有机物 。
。
 到
到 的反应方程式
的反应方程式 与
与 生成
生成 是取代反应,写出
是取代反应,写出 的结构简式
的结构简式 为原料也可合成
为原料也可合成 属于芳香族烃的同分机构体共有
属于芳香族烃的同分机构体共有 )是制药工业和电池制造业等的原料,其组成元素W、X、Y、Z是原子序数依次增大的前四周期元素;其中W、X、Y为短周期主族元素,W是元素周期表中原子半径最小的元素,X、Y同周期,且X原子和Y原子的最外层电子数之比为2∶3,
)是制药工业和电池制造业等的原料,其组成元素W、X、Y、Z是原子序数依次增大的前四周期元素;其中W、X、Y为短周期主族元素,W是元素周期表中原子半径最小的元素,X、Y同周期,且X原子和Y原子的最外层电子数之比为2∶3, 的电子数比Z原子的电子数多20.化合物甲在加热分解过程中剩余固体的质量随温度变化的曲线如图所示。下列叙述中正确的是
的电子数比Z原子的电子数多20.化合物甲在加热分解过程中剩余固体的质量随温度变化的曲线如图所示。下列叙述中正确的是
A.第一电离能: |
B.若M点时所得产物化学式为 ,则n为2 ,则n为2 |
| C.M到N的过程中只有一种气体生成 |
D. 可由 可由 与足量酸性 与足量酸性 溶液反应得到 溶液反应得到 |
 。以黄铁矿渣(含
。以黄铁矿渣(含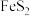 、PbS、NiS)为原料制备聚合硫酸铁流程如下。
、PbS、NiS)为原料制备聚合硫酸铁流程如下。
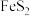 发生反应的离子方程式
发生反应的离子方程式 (水层)
(水层) (有机层)
(有机层) (有机层)
(有机层) (水层)。下列说法不正确的是_______。
(水层)。下列说法不正确的是_______。| A.可将黄铁矿渣粉碎以提高酸浸效率 |
| B.酸浸时可选择浓硫酸以提高酸浸效率 |
C.可选择 作为萃取剂 作为萃取剂 |
D.为获得 溶液可往萃取后的有机层中加稀硫酸 溶液可往萃取后的有机层中加稀硫酸 |

 中
中 的值。已知:钨酸钠可与
的值。已知:钨酸钠可与 生成蓝色物质“钨蓝”。
生成蓝色物质“钨蓝”。 和蒸馏水配成100.00mL溶液,分成两等份。
和蒸馏水配成100.00mL溶液,分成两等份。 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。 ,滴加几滴酚酞溶液,用
,滴加几滴酚酞溶液,用 的NaOH溶液滴定至终点,消耗NaOH溶液10.00mL。
的NaOH溶液滴定至终点,消耗NaOH溶液10.00mL。 中
中 的值
的值
| A.反应④有极性键的断裂与生成 |
| B.反应②③均为氧化还原反应 |
C.反应⑤的离子方程式为:Cu(NH3) +NO=N2+NH +NO=N2+NH +H2O+Cu(NH3) +H2O+Cu(NH3) |
| D.总反应还原1molNO消耗O211.2L(标准状况) |