实验一:探究温度和浓度对反应速率的影响
[实验原理及方案]在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生反应生成碘,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
实验序号 | 0.01mol/L KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol/L Na2SO3溶液的体积/mL | 水的 体积/mL | 实验 温度/℃ | 记录出现蓝色的时间/s |
① | 5 | 5 | V1 | 0 | t1 |
② | 5 | 5 | 40 | 25 | t2 |
③ | 5 | V2 | 35 | 25 | t3 |
(1)上述表格中:V1=
(2)酸性溶液中,碘酸钾和亚硫酸钠反应的离子方程式为
实验二:探究KI和FeCl3的反应存在一定的限度
[实验步骤]i.向5mL 0.01mol/L KI溶液中滴加5~6滴0.01mol/L FeCl3溶液,充分反应后,将所得溶液分成甲、乙两等份;
ii.向甲中滴加CCl4,充分振荡; iii.向乙中滴加KSCN溶液。
(3)证明反应存在一定限度的实验现象是:步骤ii中
实验三:测定反应
 的平衡常数K
的平衡常数K常温下,取2个碘量瓶分别加入下表中的试剂,振荡半小时。取一定体积的上层清液用标准Na2S2O3溶液进行滴定,测定I2和I
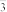 的总浓度。
的总浓度。
编号 | 250mL碘量瓶① | 250mL碘量瓶② |
试剂 | 0.5g研细的碘 60mL 0.010 mol/L KI溶液 | 0.5g研细的碘 60mL H2O |
I2和I | 0.00500 mol/L | 0.0012 mol/L |
(5)用Na2S2O3溶液滴定上层清液需要选择的指示剂为
(6)0.5g的碘不需要精确称量的理由是:在水中或KI溶液中,
(7)碘量瓶①平衡体系中
 与②中
与②中 接近,列出平衡常数K的计算式
接近,列出平衡常数K的计算式
同类型试题

y = sin x, x∈R, y∈[–1,1],周期为2π,函数图像以 x = (π/2) + kπ 为对称轴
y = arcsin x, x∈[–1,1], y∈[–π/2,π/2]
sin x = 0 ←→ arcsin x = 0
sin x = 1/2 ←→ arcsin x = π/6
sin x = √2/2 ←→ arcsin x = π/4
sin x = 1 ←→ arcsin x = π/2
y = sin x, x∈R, y∈[–1,1],周期为2π,函数图像以 x = (π/2) + kπ 为对称轴
y = arcsin x, x∈[–1,1], y∈[–π/2,π/2]
sin x = 0 ←→ arcsin x = 0
sin x = 1/2 ←→ arcsin x = π/6
sin x = √2/2 ←→ arcsin x = π/4
sin x = 1 ←→ arcsin x = π/2
 搜索
搜索

