全一卷
1.打赢蓝天保卫战,提高空气质量。下列物质不属于空气污染物的是
| A.PM2. 5 |
| B.O2 |
| C.SO2 |
| D.NO |
2.反应 可用于氯气管道的检漏。下列表示相关微粒的化学用语正确的是
可用于氯气管道的检漏。下列表示相关微粒的化学用语正确的是
 可用于氯气管道的检漏。下列表示相关微粒的化学用语正确的是
可用于氯气管道的检漏。下列表示相关微粒的化学用语正确的是A.中子数为9的氮原子: |
B.N2分子的电子式: |
| C.Cl2分子的结构式:Cl—Cl |
D.Cl-的结构示意图: |
3.下列有关物质的性质与用途具有对应关系的是
| A.铝的金属活泼性强,可用于制作铝金属制品 |
| B.氧化铝熔点高,可用作电解冶炼铝的原料 |
| C.氢氧化铝受热分解,可用于中和过多的胃酸 |
| D.明矾溶于水并水解形成胶体,可用于净水 |
4.常温下,下列各组离子在指定溶液中能大量共存的是
A. 氨水溶液:Na+、K+、OH-、NO 氨水溶液:Na+、K+、OH-、NO |
B. 盐酸溶液:Na+、K+、SO 盐酸溶液:Na+、K+、SO 、SiO 、SiO |
C. KMnO4溶液:NH KMnO4溶液:NH 、Na+、NO 、Na+、NO 、I- 、I- |
D. AgNO3溶液:NH AgNO3溶液:NH 、Mg2+、Cl-、SO 、Mg2+、Cl-、SO |
5.实验室以CaCO3为原料,制备CO2并获得CaCl2﹒6H2O晶体。下列图示装置和原理不能达到实验目的的是
A.制备CO2 |
B.收集CO2 |
C.滤去CaCO3 |
D.制得CaCl2﹒6H2O |
6.下列有关化学反应的叙述正确的是
| A.室温下,Na在空气中反应生成Na2O2 |
| B.室温下,Al与4.0 mol﹒L-1NaOH溶液反应生成NaAlO2 |
| C.室温下,Cu与浓HNO3反应放出NO气体 |
| D.室温下,Fe与浓H2SO4反应生成FeSO4 |
7.下列指定反应的离子方程式正确的是
A.Cl2通入水中制氯水: |
B.NO2通入水中制硝酸: |
C. NaAlO2溶液中通入过量CO2: NaAlO2溶液中通入过量CO2: |
D. AgNO3溶液中加入过量浓氨水: AgNO3溶液中加入过量浓氨水: |
8.反应 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是
 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是A.该反应 、 、 |
B.该反应的平衡常数 |
C.高温下反应每生成1 mol Si需消耗 |
D.用E表示键能,该反应 |
9.下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是
| A.NaOH的碱性比Mg(OH)2的强 |
| B.Cl2得到电子的能力比Br2的弱 |
C.原子半径r:  |
D.原子的最外层电子数n:  |
10.下列选项所示的物质间转化均能实现的是
A. (aq) (aq) (g) (g) 漂白粉(s) 漂白粉(s) |
B. (aq) (aq) (s) (s) (s) (s) |
C. (aq) (aq) (aq) (aq) (aq) (aq) |
D. (s) (s)  (aq) (aq) (s) (s) |
11.将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境中,下列有关说法正确的是


A.阴极的电极反应式为 |
| B.金属M的活动性比Fe的活动性弱 |
| C.钢铁设施表面因积累大量电子而被保护 |
| D.钢铁设施在河水中的腐蚀速率比在海水中的快 |
12.根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向淀粉溶液中加适量20%H2SO4溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 | 淀粉未水解 |
| B | 室温下,向 HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
| C | 室温下,向浓度均为 的BaCl2和CaCl2混合溶液中加入Na2CO3溶液,出现白色沉淀 的BaCl2和CaCl2混合溶液中加入Na2CO3溶液,出现白色沉淀 | 白色沉淀是BaCO3 |
| D | 向 H2O2溶液中滴加 H2O2溶液中滴加 KMnO4溶液,溶液褪色 KMnO4溶液,溶液褪色 | H2O2具有氧化性 |
| A.A | B.B | C.C | D.D |
13.化合物Z是合成某种抗结核候选药物的重要中间体,可由下列反应制得。

下列有关化合物X、Y和Z的说法正确的是

下列有关化合物X、Y和Z的说法正确的是
| A.X分子中不含手性碳原子 |
| B.Y分子中的碳原子一定处于同一平面 |
| C.Z在浓硫酸催化下加热可发生消去反应 |
| D.X、Z分别在过量NaOH溶液中加热,均能生成丙三醇 |
14.室温下,将两种浓度均为 的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
 的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是A. 混合溶液(pH=10.30): 混合溶液(pH=10.30): |
B.氨水-NH4Cl混合溶液(pH=9.25): |
C. 混合溶液(pH=4.76): 混合溶液(pH=4.76):  |
D. 混合溶液(pH=1.68,H2C2O4为二元弱酸): 混合溶液(pH=1.68,H2C2O4为二元弱酸):  |
15.CH4与CO2重整生成H2和CO的过程中主要发生下列反应
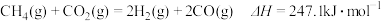

在恒压、反应物起始物质的量比 条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是

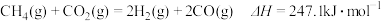

在恒压、反应物起始物质的量比
 条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
| A.升高温度、增大压强均有利于提高CH4的平衡转化率 |
| B.曲线B表示CH4的平衡转化率随温度的变化 |
| C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠 |
| D.恒压、800K、n(CH4):n(CO2)=1:1条件下,反应至CH4转化率达到X点的值,改变除温度外的特定条件继续反应,CH4转化率能达到Y点的值 |
16.吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。
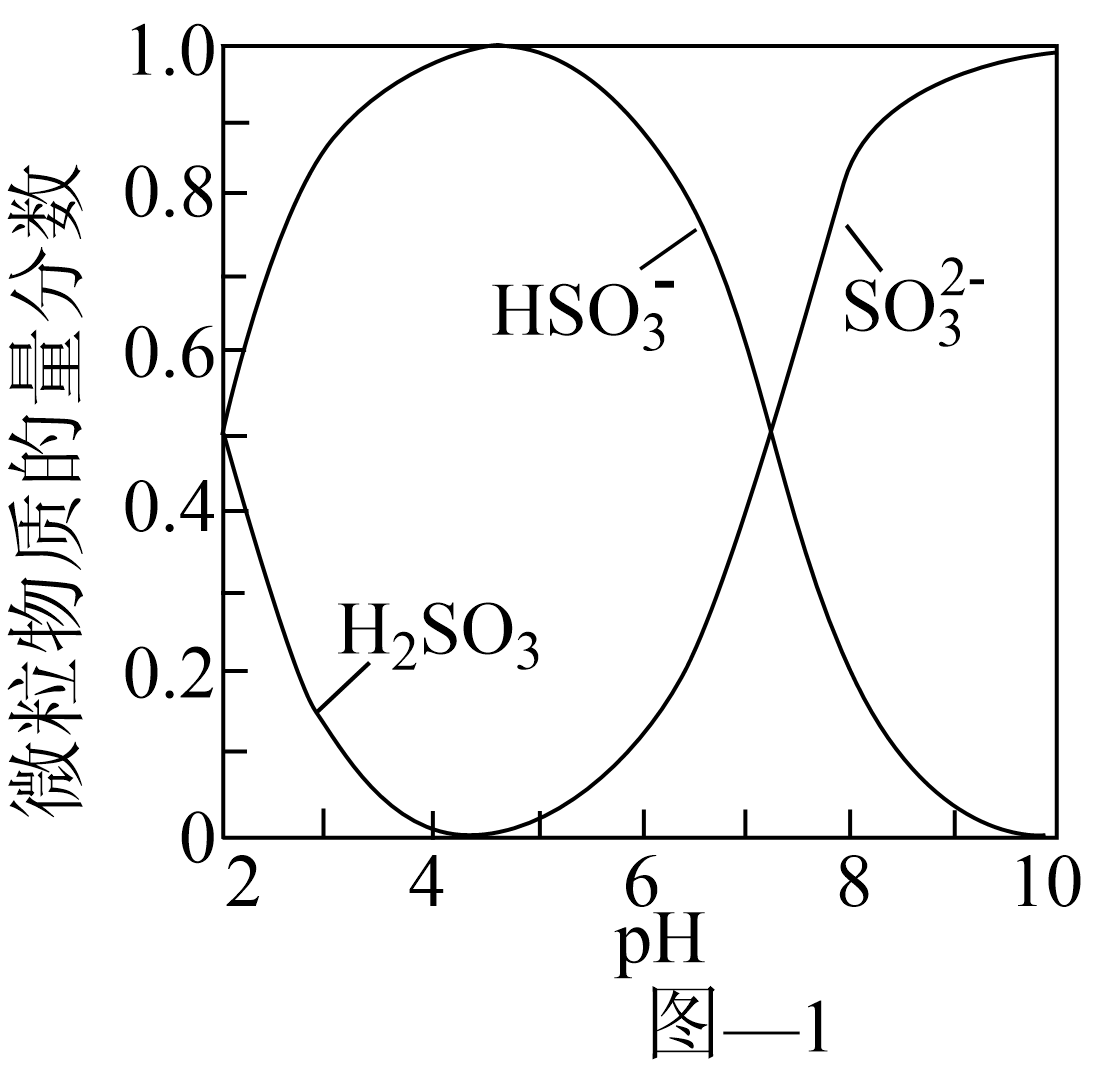
(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为___________ ;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是_____________ (填化学式)。
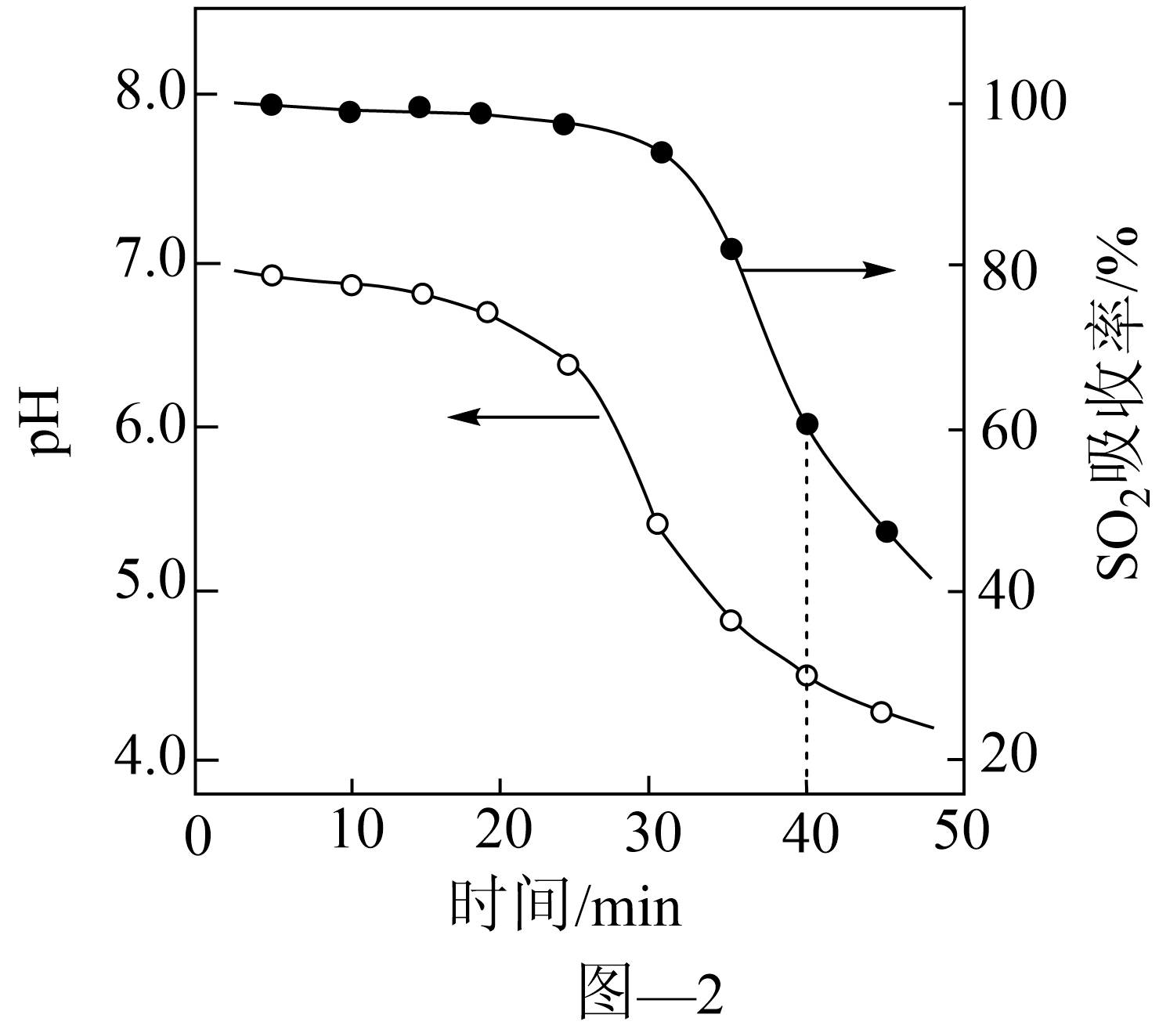
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是____________ (填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为_______________ 。
(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO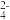 生成速率越大,其主要原因是
生成速率越大,其主要原因是__________ ;随着氧化的进行,溶液的pH将__________ (填“增大”、“减小”或“不变”)。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。

(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是

(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO
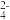 生成速率越大,其主要原因是
生成速率越大,其主要原因是17.化合物F是合成某种抗肿瘤药物的重要中间体,其合成路线如下:

(1)A中的含氧官能团名称为硝基、__________ 和____________ 。
(2)B的结构简式为______________ 。
(3)C→D的反应类型为___________ 。
(4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式________ 。
①能与FeCl3溶液发生显色反应。
②能发生水解反应,水解产物之一是α-氨基酸,另一产物分子中不同化学环境的氢原子数目比为1:1且含苯环。
(5)写出以CH3CH2CHO和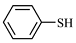 为原料制备
为原料制备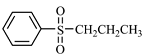 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)________ 。

(1)A中的含氧官能团名称为硝基、
(2)B的结构简式为
(3)C→D的反应类型为
(4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式
①能与FeCl3溶液发生显色反应。
②能发生水解反应,水解产物之一是α-氨基酸,另一产物分子中不同化学环境的氢原子数目比为1:1且含苯环。
(5)写出以CH3CH2CHO和
 为原料制备
为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)18.CO2/ HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
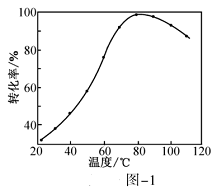
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO-,其离子方程式为__________ ;其他条件不变,HCO3-转化为HCOO-的转化率随温度的变化如图-1所示。反应温度在40℃~80℃范围内,HCO3-催化加氢的转化率迅速上升,其主要原因是_____________ 。
(2) HCOOH燃料电池。研究 HCOOH燃料电池性能的装置如图-2所示,两电极区间用允许K+、H+通过的半透膜隔开。

①电池负极电极反应式为_____________ ;放电过程中需补充的物质A为_________ (填化学式)。
②图-2所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为_______________ 。
(3) HCOOH催化释氢。在催化剂作用下, HCOOH分解生成CO2和H2可能的反应机理如图-3所示。

①HCOOD催化释氢反应除生成CO2外,还生成__________ (填化学式)。
②研究发现:其他条件不变时,以 HCOOK溶液代替 HCOOH催化释氢的效果更佳,其具体优点是_______________ 。

(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO-,其离子方程式为
(2) HCOOH燃料电池。研究 HCOOH燃料电池性能的装置如图-2所示,两电极区间用允许K+、H+通过的半透膜隔开。

①电池负极电极反应式为
②图-2所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为
(3) HCOOH催化释氢。在催化剂作用下, HCOOH分解生成CO2和H2可能的反应机理如图-3所示。

①HCOOD催化释氢反应除生成CO2外,还生成
②研究发现:其他条件不变时,以 HCOOK溶液代替 HCOOH催化释氢的效果更佳,其具体优点是
19.以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵【(NH4)3Fe(C6H5O7)2】。
(1)Fe基态核外电子排布式为___________ ;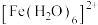 中与Fe2+配位的原子是
中与Fe2+配位的原子是________ (填元素符号)。
(2)NH3分子中氮原子的轨道杂化类型是____________ ;C、N、O元素的第一电离能由大到小的顺序为_______________ 。
(3)与NH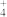 互为等电子体的一种分子为
互为等电子体的一种分子为_______________ (填化学式)。
(4)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_________ mol。
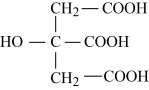
(1)Fe基态核外电子排布式为
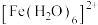 中与Fe2+配位的原子是
中与Fe2+配位的原子是(2)NH3分子中氮原子的轨道杂化类型是
(3)与NH
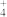 互为等电子体的一种分子为
互为等电子体的一种分子为(4)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为
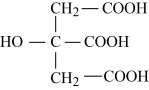
20.次氯酸钠溶液和二氯异氰尿酸钠(C3N3O3Cl2Na)都是常用的杀菌消毒剂。 NaClO可用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为__________ ;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是__________________ 。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为

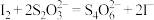
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①通过计算判断该样品是否为优质品_______ 。(写出计算过程,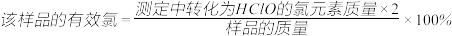 )
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________ (填“偏高”或“偏低”)。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为


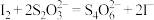
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用
 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。①通过计算判断该样品是否为优质品
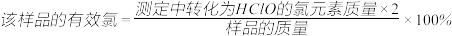 )
)②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
21.实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料α-Fe2O3。
其主要实验流程如下:

(1)酸浸:用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下列措施能提高铁元素浸出率的有___________ (填序号)。
A.适当升高酸浸温度
B.适当加快搅拌速度
C.适当缩短酸浸时间
(2)还原:向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程中除生成Fe2+外,还会生成___________ (填化学式);检验Fe3+是否还原完全的实验操作是______________ 。
(3)除杂:向“还原”后的滤液中加入NH4F溶液,使Ca2+转化为CaF2沉淀除去。若溶液的pH偏低、将会导致CaF2沉淀不完全,其原因是___________ [ ,
,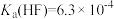 ]。
]。
(4)沉铁:将提纯后的FeSO4溶液与氨水-NH4HCO3混合溶液反应,生成FeCO3沉淀。
①生成FeCO3沉淀的离子方程式为____________ 。
②设计以FeSO4溶液、氨水- NH4HCO3混合溶液为原料,制备FeCO3的实验方案:__ 。
【FeCO3沉淀需“洗涤完全”,Fe(OH)2开始沉淀的pH=6.5】。
其主要实验流程如下:

(1)酸浸:用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下列措施能提高铁元素浸出率的有
A.适当升高酸浸温度
B.适当加快搅拌速度
C.适当缩短酸浸时间
(2)还原:向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程中除生成Fe2+外,还会生成
(3)除杂:向“还原”后的滤液中加入NH4F溶液,使Ca2+转化为CaF2沉淀除去。若溶液的pH偏低、将会导致CaF2沉淀不完全,其原因是
 ,
,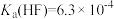 ]。
]。(4)沉铁:将提纯后的FeSO4溶液与氨水-NH4HCO3混合溶液反应,生成FeCO3沉淀。
①生成FeCO3沉淀的离子方程式为
②设计以FeSO4溶液、氨水- NH4HCO3混合溶液为原料,制备FeCO3的实验方案:
【FeCO3沉淀需“洗涤完全”,Fe(OH)2开始沉淀的pH=6.5】。
22.羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。制备少量羟基乙酸钠的反应为

实验步骤如下:

步骤1:如图所示装置的反应瓶中,加入40g氯乙酸、50mL水,搅拌。逐步加入40%NaOH溶液,在95℃继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是___________;逐步加入NaOH溶液的目的是____________。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是_______________。
(3)步骤3中,粗产品溶解于过量水会导致产率__________(填“增大”或“减小”);去除活性炭的操作名称是_______________。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是_______________。

实验步骤如下:

步骤1:如图所示装置的反应瓶中,加入40g氯乙酸、50mL水,搅拌。逐步加入40%NaOH溶液,在95℃继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是___________;逐步加入NaOH溶液的目的是____________。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是_______________。
(3)步骤3中,粗产品溶解于过量水会导致产率__________(填“增大”或“减小”);去除活性炭的操作名称是_______________。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是_______________。
 搜索
搜索
 难度系数:0.94
难度系数:0.94  答案解析
答案解析
 有奖纠错
有奖纠错
