全一卷
1.中国五千年文明历史中蕴藏了丰富的化学知识,下列说法错误的是
| A.毛笔中“狼毫”的主要成分为蛋白质 | B.宣纸的主要成分为纤维素 |
| C.丝绸的主要成分属于天然高分子化合物 | D.古代汉服的主要制作材料为涤纶 |
2.下列化学用语的使用错误的是
| A.乙酸的分子式为CH3COOH | B. 和 和 分子中所含碳原子数相同 分子中所含碳原子数相同 |
C.乙烯的比例模型为 | D.甘氨酸的球棍模型为 |
3.下列固体分类中正确的一组是
| | 离子晶体 | 共价晶体 | 分子晶体 |
A | 苏打 | 金刚砂 | 干冰 |
B | 玻璃 |
| 硫磺 |
C |
| 石墨 | 冰醋酸 |
D | 胆矾 | 金刚石 |
|
| A.A | B.B | C.C | D.D |
4.下列有机物中,只需要用水就可以鉴别的是
| A.环己烷、苯、乙醇 | B.四氯化碳、苯、甘油 |
| C.四氯化碳、溴乙烷、乙酸 | D.环己烷、乙二醇、甘油 |
5.乙醇在下列反应中没有断裂O-H键的是
| A.加热条件下与HBr溶液反应 | B.Cu做催化剂条件下发生催化氧化 |
| C.浓H2SO4条件下发生分子间脱水 | D.浓H2SO4条件下与乙酸发生酯化反应 |
6.下列物质之间的关系与微粒半径大小无关的是
A.熔点: | B.熔点:金刚石>硅单质 |
| C.沸点:水晶>氯化锂 | D.热分解所需温度: |
7.有机反应副反应较多,下列有机反应的产物中一定存在同分异构现象(不考虑立体异构)的是
A.甲烷与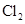 光照条件下的反应 光照条件下的反应 |
B. 与 与 的加成反应 的加成反应 |
C. 在 在 水溶液中加热反应 水溶液中加热反应 |
D. 与 与 的乙醇溶液共热反应 的乙醇溶液共热反应 |
8.环已基苯(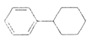 )常用作高沸点溶剂和渗透剂,可用于有机合成。下列关于环己基苯的说法错误的是
)常用作高沸点溶剂和渗透剂,可用于有机合成。下列关于环己基苯的说法错误的是
 )常用作高沸点溶剂和渗透剂,可用于有机合成。下列关于环己基苯的说法错误的是
)常用作高沸点溶剂和渗透剂,可用于有机合成。下列关于环己基苯的说法错误的是| A.属于芳香烃 | B.所有碳原子可能共平面 |
| C.可发生加成反应、取代反应和氧化反应 | D.一氯代物有7种(不考虑立体异构) |
9.下列关于离子晶体的说法正确的是
| A.形成离子晶体的阴、阳离子之间只存在静电引力 |
| B.阴、阳离子的配位数只与阴、阳离子的角标比有关 |
| C.离子化合物的熔点一定比共价化合物的熔点高 |
| D.熔融状态离子键被破坏,使离子自由移动能导电 |
10.实验室制备乙酸乙酯的装置图如下。下列说法正确的是
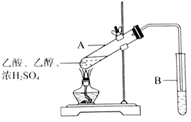

| A.浓硫酸能加快酯化反应速率 |
| B.将乙酸和乙醇的混合液加入浓硫酸中,边加边振荡 |
| C.将试管B中混合液直接蒸馏可得较纯的乙酸乙酯 |
D.为除去挥发的醋酸,试管B中可盛放较浓的 溶液 溶液 |
11.设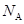 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
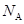 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中所含共价键数目为 中所含共价键数目为 |
B.标准状况下, 环己烷中所含碳原子数目为 环己烷中所含碳原子数目为 |
C. 乙酸乙酯和乙醛的混合物充分燃烧,消耗氧气分子数目为 乙酸乙酯和乙醛的混合物充分燃烧,消耗氧气分子数目为 |
D. 乙醇溶液与足量 乙醇溶液与足量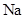 反应生成氢气分子数为 反应生成氢气分子数为 |
12.有机物a(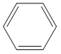 )、b(
)、b(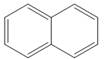 )、c(
)、c(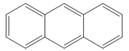 )……,属于一个系列,下列说法错误的是
)……,属于一个系列,下列说法错误的是
 )、b(
)、b( )、c(
)、c( )……,属于一个系列,下列说法错误的是
)……,属于一个系列,下列说法错误的是| A.该系列分子中所有原子共平面 |
B.该系列有机物的通式可表示为 |
| C.c的二氯取代物有15种 |
D.等质量a、b、c与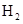 发生加成反应消耗 发生加成反应消耗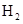 量最多的是a 量最多的是a |
13.已知 的熔点为2700℃,其晶胞结构如图所示。下列说法错误的是
的熔点为2700℃,其晶胞结构如图所示。下列说法错误的是
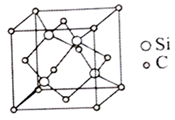
 的熔点为2700℃,其晶胞结构如图所示。下列说法错误的是
的熔点为2700℃,其晶胞结构如图所示。下列说法错误的是
A. 晶体中碳原子和硅原子均采用 晶体中碳原子和硅原子均采用 杂化 杂化 |
| B.硅单质的熔点高于2700℃ |
| C.距离硅原子最近的硅原子数为4 |
D.若晶胞参数为 ,则该晶体的密度为 ,则该晶体的密度为 |
14.烯烃的加成反应是有机合成中的重要环节,几种有机物的转化关系如下,下列说法错误的是
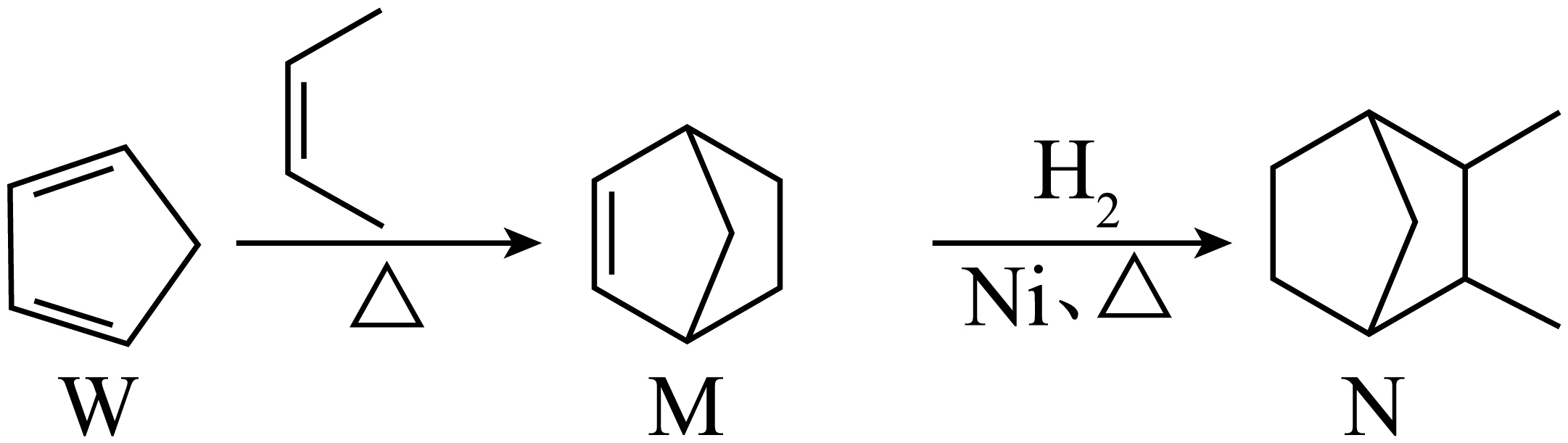

| A.W中所有原子可能处于同一平面 | B.M的分子式为 |
| C.上述两个转化过程均为加成反应 | D.N的一氯代物有5种(不含立体异构) |
15.下列实验操作及现象所得实验结论正确的是
| 选项 | 实验操作及现象 | 实验结论 |
A | 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 | 氯代烷溶于水显酸性 |
B | 向某卤代烃中加入 溶液,加热一段时间后冷却;加入足量稀硝酸酸化,再滴加 溶液,加热一段时间后冷却;加入足量稀硝酸酸化,再滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 | 该卤代烃中含有氯原子 |
C | 加热乙醇和浓硫酸的混合物,产生能使酸性 溶液褪色的气体 溶液褪色的气体 | 乙醇发生消去反应生成乙烯 |
D | 向麦芽糖中加入稀硫酸,一段时间后,加 溶液调至碱性,再加入银氨溶液,水浴加热,有银镜产生 溶液调至碱性,再加入银氨溶液,水浴加热,有银镜产生 | 麦芽糖已经水解 |
| A.A | B.B | C.C | D.D |
16.碱金属元素形成的单质及其化合物有广泛的应用。回答下列问题:
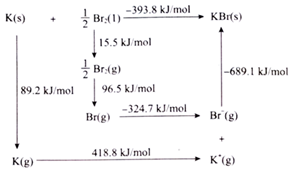
(1)K与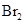 反应可形成离子晶体
反应可形成离子晶体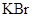 ,其离子键形成的
,其离子键形成的 循环如图所示。可知,K原子的第一电离能为
循环如图所示。可知,K原子的第一电离能为______ 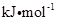 ,
,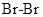 键键能为
键键能为_____ 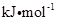 。
。
(2)K与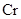 属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为
属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为________ 。
(3)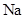 与
与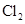 在高压下可以形成组成和结构均不相同的晶体。下图是其中一种晶体的晶胞。则该晶体的化学式为
在高压下可以形成组成和结构均不相同的晶体。下图是其中一种晶体的晶胞。则该晶体的化学式为__________ 。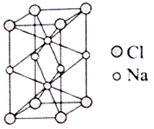
(1)K与
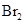 反应可形成离子晶体
反应可形成离子晶体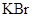 ,其离子键形成的
,其离子键形成的 循环如图所示。可知,K原子的第一电离能为
循环如图所示。可知,K原子的第一电离能为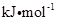 ,
,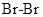 键键能为
键键能为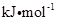 。
。
(2)K与
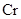 属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为
属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为(3)
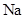 与
与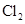 在高压下可以形成组成和结构均不相同的晶体。下图是其中一种晶体的晶胞。则该晶体的化学式为
在高压下可以形成组成和结构均不相同的晶体。下图是其中一种晶体的晶胞。则该晶体的化学式为
17.以下几种有机物是重要的化工原料。回答下列问题:
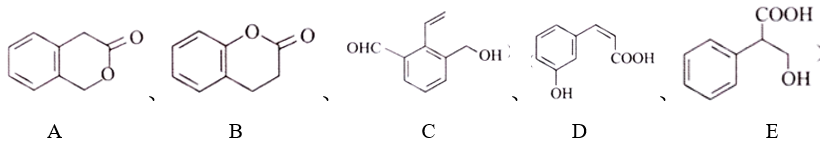
(1)A的分子式为_______ ;上述有机物中与A互为同分异构体的是_______ (填选项字母)。
(2)C、D中均存在碳碳双键,其中存在顺反异构的是_________ (填选项字母);C与银氨溶液反应的化学方程式为_______ 。
(3)B在 溶液中水解的化学方程式为
溶液中水解的化学方程式为________ 。
(4)下列试剂可以用来鉴别D和E的是________ (填选项字母)。
a.溴水 b.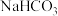 溶液 c.
溶液 c.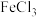 溶液 d.酸性
溶液 d.酸性 溶液
溶液
(5)E在一定条件下发生缩聚反应的化学方程式为_______ 。

(1)A的分子式为
(2)C、D中均存在碳碳双键,其中存在顺反异构的是
(3)B在
 溶液中水解的化学方程式为
溶液中水解的化学方程式为(4)下列试剂可以用来鉴别D和E的是
a.溴水 b.
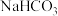 溶液 c.
溶液 c.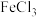 溶液 d.酸性
溶液 d.酸性 溶液
溶液(5)E在一定条件下发生缩聚反应的化学方程式为
18.乙酸异丙酯呈水果香气,主要用作涂料、印刷油墨等的溶剂,也是药物生产中的萃取剂及香料组分。实验室用冰醋酸和异丙醇(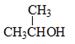 )制备乙酸异丙酯,有关物质的相关信息如下表所示:
)制备乙酸异丙酯,有关物质的相关信息如下表所示:
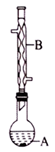
实验装置如图:
实验操作如下:
合成:在圆底烧瓶中将6.00mL的冰醋酸和3.00mL浓硫酸混合,再加入15.00mL的异丙醇,摇匀后加入几粒沸石,加热反应2h后,将反应物冷却至室温。
分离和提纯:将反应后A中液体分离出来后,分别用适量水、10%Na2CO3溶液、饱和NaCl溶液洗涤;最后转移至锥形瓶,加入无水氯化钙干燥。
精制:将干燥后的粗品蒸馏,收集馏分;得到产品体积为10.20mL。
(1)仪器B的名称为____,使用时应从_____(填“上”或“下”)口进冷水,仪器A的容积最适合的为_____(填标号)。
A.25mL B.50mL C.250mL D.500mL
(2)合成过程中发生反应的化学方程式为______。
(3)混合中加入过量异丙醇的目的为_____。
(4)分离和提纯过程中洗涤操作应在____(填仪器名称)中进行,用10%Na2CO3溶液洗涤的目的是_____。
(5)精制过程中蒸馏时应选择装置_____(填标号),收集_____℃的馏分。
A.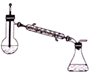 B.
B.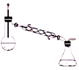 C.
C. D.
D.
(6)该实验产品的产率为_____%(保留两位有效数字)。
 )制备乙酸异丙酯,有关物质的相关信息如下表所示:
)制备乙酸异丙酯,有关物质的相关信息如下表所示:| | 乙酸 | 异丙醇 | 乙酸异丙酯 |
密度/ | 1.05 | 0.79 | 0.87 |
| 沸点/℃ | 118.3 | 82.5 | 88.4 |
| 水溶性 | 互溶 | 互溶 | 微溶 |
| 相对分子质量 | 60 | 60 | 102 |
实验装置如图:

实验操作如下:
合成:在圆底烧瓶中将6.00mL的冰醋酸和3.00mL浓硫酸混合,再加入15.00mL的异丙醇,摇匀后加入几粒沸石,加热反应2h后,将反应物冷却至室温。
分离和提纯:将反应后A中液体分离出来后,分别用适量水、10%Na2CO3溶液、饱和NaCl溶液洗涤;最后转移至锥形瓶,加入无水氯化钙干燥。
精制:将干燥后的粗品蒸馏,收集馏分;得到产品体积为10.20mL。
(1)仪器B的名称为____,使用时应从_____(填“上”或“下”)口进冷水,仪器A的容积最适合的为_____(填标号)。
A.25mL B.50mL C.250mL D.500mL
(2)合成过程中发生反应的化学方程式为______。
(3)混合中加入过量异丙醇的目的为_____。
(4)分离和提纯过程中洗涤操作应在____(填仪器名称)中进行,用10%Na2CO3溶液洗涤的目的是_____。
(5)精制过程中蒸馏时应选择装置_____(填标号),收集_____℃的馏分。
A.
 B.
B. C.
C. D.
D.
(6)该实验产品的产率为_____%(保留两位有效数字)。
19.铜是人类知道最早的金属之一。回答下列问题:
(1)基态铜原子价层电子排布图为____ ,其核外占据最高能层电子的电子云轮廓图的形状为____ 。
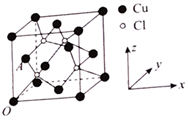
(2)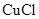 晶胞结构如下图所示。
晶胞结构如下图所示。
①区别晶体与非晶体最科学的方法是_____ ;该晶胞中铜原子的配位数为_____ 。
②若位于O点的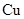 原子的坐标为(0,0,0),A点的Cu原子的坐标为(0,
原子的坐标为(0,0,0),A点的Cu原子的坐标为(0,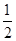 ,
,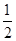 ),则晶胞中距离O点最近的
),则晶胞中距离O点最近的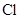 原子的坐标为
原子的坐标为____ 。
(3)某铜氧化合物是一种杀菌剂和陶瓷的着色剂,其立方晶胞如图所示。
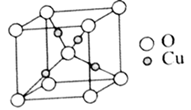
①该铜氧化合物的化学式为___ 。
②若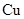 原子之间最短距离为
原子之间最短距离为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为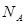 ,该晶体的密度为
,该晶体的密度为____ 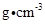 (列出计算式即可)。
(列出计算式即可)。
(1)基态铜原子价层电子排布图为
(2)
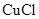 晶胞结构如下图所示。
晶胞结构如下图所示。①区别晶体与非晶体最科学的方法是
②若位于O点的
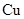 原子的坐标为(0,0,0),A点的Cu原子的坐标为(0,
原子的坐标为(0,0,0),A点的Cu原子的坐标为(0,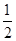 ,
,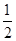 ),则晶胞中距离O点最近的
),则晶胞中距离O点最近的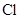 原子的坐标为
原子的坐标为
(3)某铜氧化合物是一种杀菌剂和陶瓷的着色剂,其立方晶胞如图所示。

①该铜氧化合物的化学式为
②若
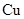 原子之间最短距离为
原子之间最短距离为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为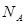 ,该晶体的密度为
,该晶体的密度为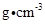 (列出计算式即可)。
(列出计算式即可)。20.有机物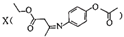 是合成某药品的中间体,利用芳香化合物M和酯类化合物N合成X的一种路线如下:
是合成某药品的中间体,利用芳香化合物M和酯类化合物N合成X的一种路线如下:
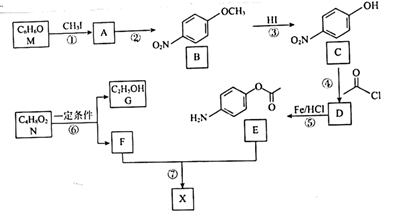
已知:i.2N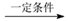 F+C2H5OH
F+C2H5OH
ii.F+E→X+H2O
回答下列问题:
(1)C的名称为___ ;F中含氧官能团的名称为____ 。
(2)反应②所需试剂及反应条件分别为____ ;反应⑤的反应类型为____ 。
(3)反应④的化学反应方程式为____ 。
(4)在合成路线中设计反应①和反应③的目的为____ 。
(5)满足下列条件的E的同分异构体有_____ 种,任写一种核磁共振氢谱为5组峰,峰面积之比为2:2:2:2:1的结构简式______ 。
a.属于芳香族化合物 b.含有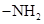 c.能与
c.能与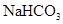 溶液反应
溶液反应
(6)参照上述合成路线,设计以苯和丁酮为原料制备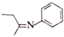 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)___ 。
 是合成某药品的中间体,利用芳香化合物M和酯类化合物N合成X的一种路线如下:
是合成某药品的中间体,利用芳香化合物M和酯类化合物N合成X的一种路线如下:
已知:i.2N
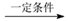 F+C2H5OH
F+C2H5OHii.F+E→X+H2O
回答下列问题:
(1)C的名称为
(2)反应②所需试剂及反应条件分别为
(3)反应④的化学反应方程式为
(4)在合成路线中设计反应①和反应③的目的为
(5)满足下列条件的E的同分异构体有
a.属于芳香族化合物 b.含有
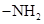 c.能与
c.能与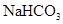 溶液反应
溶液反应(6)参照上述合成路线,设计以苯和丁酮为原料制备
 的合成路线(无机试剂任选)
的合成路线(无机试剂任选) 搜索
搜索
 难度系数:0.00
难度系数:0.00  答案解析
答案解析
 有奖纠错
有奖纠错



