全一卷
1.化学在人类社会发展中发挥着重要作用,下列事实不涉及 化学反应的是
| A.利用废弃的秸秆生产生物质燃料乙醇 |
| B.利用石油生产塑料、化纤等高分子材料 |
| C.利用基本的化学原料生产化学合成药物 |
| D.利用反渗透膜从海水中分离出淡水 |
2.下列离子方程式能用来解释相应实验现象的是
| 实验现象 | 离子方程式 | |
| A | 向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 |  |
| B | 向沸水中滴加饱和氯化铁溶液得到红褐色液体 |  |
| C | 二氧化硫使酸性高锰酸钾溶液褪色 |  |
| D | 氧化亚铁溶于稀硝酸 |  |
| A.A | B.B | C.C | D.D |
3.下列有关金属及其化合物的不合理 的是
A.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
| B.铝中添加适量钾,制得低密度、高强度的铝合金,可用于航空工业 |
C.盐碱地(含较多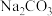 等)不利于作物生长,可施加熟石灰进行改良 等)不利于作物生长,可施加熟石灰进行改良 |
D.无水 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水 |
4.下列实验操作或装置能达到目的的是
| A | B | C | D |
 |  |  |  |
| 混合浓硫酸和乙醇 | 配制一定浓度的溶液 | 收集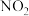 气体 气体 | 证明乙炔可使溴水褪色 |
| A.A | B.B | C.C | D.D |
5.某温度下, 和
和 的电离常数分别为
的电离常数分别为 和
和 。将
。将 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其 随加水体积的变化如图所示。下列叙述正确的是
随加水体积的变化如图所示。下列叙述正确的是

 和
和 的电离常数分别为
的电离常数分别为 和
和 。将
。将 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其 随加水体积的变化如图所示。下列叙述正确的是
随加水体积的变化如图所示。下列叙述正确的是
A.曲线Ⅰ代表 溶液 溶液 |
| B.溶液中水的电离程度:b点>c点 |
C.从c点到d点,溶液中 保持不变(其中 保持不变(其中 、 、 分别代表相应的酸和酸根离子) 分别代表相应的酸和酸根离子) |
D.相同体积a点的两溶液分别与 恰好中和后,溶液中 恰好中和后,溶液中 相同 相同 |
6.我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是


A.放电时,a电极反应为 |
| B.放电时,溶液中离子的数目增大 |
C.充电时,b电极每增重 ,溶液中有 ,溶液中有 被氧化 被氧化 |
| D.充电时,a电极接外电源负极 |
7.氮、磷、砷 、锑
、锑 、铋
、铋 、镆
、镆 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置______ 。 的中子数为
的中子数为______ 。
已知: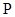 (
( ,白磷)=
,白磷)=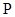 (
( ,黑磷)
,黑磷)  ;
;
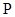 (
( ,白磷)=
,白磷)=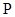 (
( ,红磷)
,红磷)  ;
;
由此推知,其中最稳定的磷单质是______ 。
(2)氮和磷氢化物性质的比较:热稳定性:
______  (填“>”“<”)。
(填“>”“<”)。
沸点:
______  (填“>”“<”),判断依据是
(填“>”“<”),判断依据是______ 。
(3) 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是______ (填序号)。
a.不能与 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应
(4) 能发生较强烈的水解,生成难溶的
能发生较强烈的水解,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式_______________________ ,因此,配制 溶液应注意
溶液应注意_______________________ 。
(5)在1L真空密闭容器中加入a mol PH4I固体,t℃时发生如下反应:
 ①
①
 ②
②
 ③
③
达平衡时,体系中 ,
, ,
, ,则
,则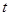 ℃时反应①的平衡常数
℃时反应①的平衡常数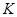 值为
值为______ (用字母表示)。
 、锑
、锑 、铋
、铋 、镆
、镆 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:(1)砷在元素周期表中的位置
 的中子数为
的中子数为已知:
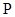 (
( ,白磷)=
,白磷)=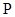 (
( ,黑磷)
,黑磷)  ;
;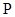 (
( ,白磷)=
,白磷)=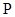 (
( ,红磷)
,红磷)  ;
;由此推知,其中最稳定的磷单质是
(2)氮和磷氢化物性质的比较:热稳定性:

 (填“>”“<”)。
(填“>”“<”)。沸点:

 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(3)
 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是a.不能与
 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应(4)
 能发生较强烈的水解,生成难溶的
能发生较强烈的水解,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式 溶液应注意
溶液应注意(5)在1L真空密闭容器中加入a mol PH4I固体,t℃时发生如下反应:
 ①
① ②
② ③
③达平衡时,体系中
 ,
, ,
, ,则
,则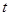 ℃时反应①的平衡常数
℃时反应①的平衡常数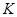 值为
值为8.我国化学家首次实现了膦催化的 环加成反应,并依据该反应,发展了一条合成中草药活性成分茅苍术醇的有效路线。
环加成反应,并依据该反应,发展了一条合成中草药活性成分茅苍术醇的有效路线。
已知 环加成反应:
环加成反应:

( 、
、 可以是
可以是 或
或 )
)

回答下列问题:
(1)茅苍术醇的分子式为____________ ,所含官能团名称为____________ ,分子中手性碳原子(连有四个不同的原子或原子团)的数目为____________ 。
(2)化合物B的核磁共振氢谱中有______ 个吸收峰;其满足以下条件的同分异构体(不考虑手性异构)数目为______ 。
①分子中含有碳碳叁键和乙酯基
②分子中有连续四个碳原子在一条直线上
写出其中碳碳叁键和乙酯基直接相连的同分异构体的结构简式____________ 。
(3) 的反应类型为
的反应类型为____________ 。
(4) 的化学方程式为
的化学方程式为__________________ ,除 外该反应另一产物的系统命名为
外该反应另一产物的系统命名为____________ 。
(5)下列试剂分别与 和
和 反应,可生成相同环状产物的是
反应,可生成相同环状产物的是______ (填序号)。
a.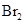 b.
b. c.
c. 溶液
溶液
(6)参考以上合成路线及条件,选择两种链状不饱和酯,通过两步反应合成化合物 ,在方框中写出路线流程图(其他试剂任选)。
,在方框中写出路线流程图(其他试剂任选)。_______

 环加成反应,并依据该反应,发展了一条合成中草药活性成分茅苍术醇的有效路线。
环加成反应,并依据该反应,发展了一条合成中草药活性成分茅苍术醇的有效路线。已知
 环加成反应:
环加成反应:

(
 、
、 可以是
可以是 或
或 )
)
回答下列问题:
(1)茅苍术醇的分子式为
(2)化合物B的核磁共振氢谱中有
①分子中含有碳碳叁键和乙酯基

②分子中有连续四个碳原子在一条直线上
写出其中碳碳叁键和乙酯基直接相连的同分异构体的结构简式
(3)
 的反应类型为
的反应类型为(4)
 的化学方程式为
的化学方程式为 外该反应另一产物的系统命名为
外该反应另一产物的系统命名为(5)下列试剂分别与
 和
和 反应,可生成相同环状产物的是
反应,可生成相同环状产物的是a.
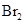 b.
b. c.
c. 溶液
溶液(6)参考以上合成路线及条件,选择两种链状不饱和酯,通过两步反应合成化合物
 ,在方框中写出路线流程图(其他试剂任选)。
,在方框中写出路线流程图(其他试剂任选)。
9.环己烯是重要的化工原料。其实验室制备流程如下:

回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为____________ ,现象为__________________ 。
(2)操作1的装置如图所示(加热和夹持装置已略去)。

①烧瓶A中进行的可逆反应化学方程式为________________________ ,浓硫酸也可作该反应的催化剂,选择 而不用浓硫酸的原因为
而不用浓硫酸的原因为________________________ (填序号)。
a.浓硫酸易使原料碳化并产生
b. 污染小、可循环使用,符合绿色化学理念
污染小、可循环使用,符合绿色化学理念
c.同等条件下,用 比浓硫酸的平衡转化率高
比浓硫酸的平衡转化率高
②仪器B的作用为____________ 。
(3)操作2用到的玻璃仪器是____________ 。
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,____________ ,弃去前馏分,收集83℃的馏分。
Ⅱ.环己烯含量的测定
在一定条件下,向 环己烯样品中加入定量制得的
环己烯样品中加入定量制得的 ,与环己烯充分反应后,剩余的
,与环己烯充分反应后,剩余的 与足量
与足量 作用生成
作用生成 ,用
,用 的
的 标准溶液滴定,终点时消耗
标准溶液滴定,终点时消耗 标准溶液
标准溶液 (以上数据均已扣除干扰因素)。
(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①
②
③
(5)滴定所用指示剂为____________ 。样品中环己烯的质量分数为____________ (用字母表示)。
(6)下列情况会导致测定结果偏低的是____________ (填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c. 标准溶液部分被氧化
标准溶液部分被氧化

回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为
(2)操作1的装置如图所示(加热和夹持装置已略去)。

①烧瓶A中进行的可逆反应化学方程式为
 而不用浓硫酸的原因为
而不用浓硫酸的原因为a.浓硫酸易使原料碳化并产生

b.
 污染小、可循环使用,符合绿色化学理念
污染小、可循环使用,符合绿色化学理念c.同等条件下,用
 比浓硫酸的平衡转化率高
比浓硫酸的平衡转化率高②仪器B的作用为
(3)操作2用到的玻璃仪器是
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,
Ⅱ.环己烯含量的测定
在一定条件下,向
 环己烯样品中加入定量制得的
环己烯样品中加入定量制得的 ,与环己烯充分反应后,剩余的
,与环己烯充分反应后,剩余的 与足量
与足量 作用生成
作用生成 ,用
,用 的
的 标准溶液滴定,终点时消耗
标准溶液滴定,终点时消耗 标准溶液
标准溶液 (以上数据均已扣除干扰因素)。
(以上数据均已扣除干扰因素)。测定过程中,发生的反应如下:
①

②

③

(5)滴定所用指示剂为
(6)下列情况会导致测定结果偏低的是
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.
 标准溶液部分被氧化
标准溶液部分被氧化10.多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。

回答下列问题:
Ⅰ.硅粉与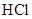 在300℃时反应生成
在300℃时反应生成 气体和
气体和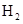 ,放出
,放出 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为________________________ 。 的电子式为
的电子式为__________________ 。
Ⅱ.将 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①

②

③

(1)氢化过程中所需的高纯度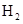 可用惰性电极电解
可用惰性电极电解 溶液制备,写出产生
溶液制备,写出产生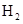 的电极名称
的电极名称______ (填“阳极”或“阴极”),该电极反应方程式为________________________ 。

(2)已知体系自由能变 ,
, 时反应自发进行。三个氢化反应的
时反应自发进行。三个氢化反应的 与温度的关系如图1所示,可知:反应①能自发进行的最低温度是
与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________ ;相同温度下,反应②比反应①的 小,主要原因是
小,主要原因是________________________ 。
(3)不同温度下反应②中 转化率如图2所示。下列叙述正确的是
转化率如图2所示。下列叙述正确的是______ (填序号)。
a.B点: b.
b. :A点
:A点 点 c.反应适宜温度:
点 c.反应适宜温度: ℃
℃
(4)反应③的
______ (用 ,
, 表示)。温度升高,反应③的平衡常数
表示)。温度升高,反应③的平衡常数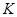
______ (填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除 、
、 和
和 外,还有
外,还有______ (填分子式)。

回答下列问题:
Ⅰ.硅粉与
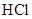 在300℃时反应生成
在300℃时反应生成 气体和
气体和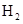 ,放出
,放出 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为 的电子式为
的电子式为Ⅱ.将
 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:①


②


③


(1)氢化过程中所需的高纯度
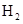 可用惰性电极电解
可用惰性电极电解 溶液制备,写出产生
溶液制备,写出产生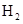 的电极名称
的电极名称
(2)已知体系自由能变
 ,
, 时反应自发进行。三个氢化反应的
时反应自发进行。三个氢化反应的 与温度的关系如图1所示,可知:反应①能自发进行的最低温度是
与温度的关系如图1所示,可知:反应①能自发进行的最低温度是 小,主要原因是
小,主要原因是(3)不同温度下反应②中
 转化率如图2所示。下列叙述正确的是
转化率如图2所示。下列叙述正确的是a.B点:
 b.
b. :A点
:A点 点 c.反应适宜温度:
点 c.反应适宜温度: ℃
℃(4)反应③的

 ,
, 表示)。温度升高,反应③的平衡常数
表示)。温度升高,反应③的平衡常数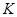
(5)由粗硅制备多晶硅过程中循环使用的物质除
 、
、 和
和 外,还有
外,还有 搜索
搜索
 难度系数:0.94
难度系数:0.94  答案解析
答案解析
 有奖纠错
有奖纠错
