全一卷
1.下列实验操作规范的是
A.点燃酒精灯 | B.装固体粉末 |
C.滴加液体 | D.测溶液的pH |
2.中国科学院首创室温制氢方案,其反应原理如图所示。下列说法错误的是


A.该反应的化学方程式是CO+H2O H2+CO2 H2+CO2 |
| B.该反应前后分子数目不变 |
| C.该反应前后氢元素的化合价不变 |
| D.反应物CO和H2O都是氧化物 |
3.20℃时,将45g氯化钠均分成五份,依次加入到盛有100g水的烧杯中,充分溶解。实验数据如下表:
下列分析正确的是
| 实验序号 | ① | ② | ③ | ④ | ⑤ |
| 氯化钠质量/g | 9 | 18 | 27 | 36 | 45 |
| 溶液质量/g | 109 | 118 | 127 | 136 | 136 |
| A.实验③所得溶液的溶质质量分数最大 |
| B.实验④所得溶液是氯化钠的不饱和溶液 |
| C.20℃时,氯化钠的溶解度为36g/100g 水 |
| D.将实验①所得溶液蒸发50g水,冷却到20℃,溶液达到饱和 |
4.下列实验方案不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别酱油和食醋 | 闻气味 |
| B | 检验氢氧化钠是否变质 | 溶于水,滴加酚酞试液 |
| C | 探究水的组成 | 检验水电解后产生的气体 |
| D | 粗盐提纯 | 溶解、过滤、蒸发 |
| A.A | B.B | C.C | D.D |
5.将锌粉持续加入到100g含有AgNO3和Cu(NO3)2两种溶质的混合溶液中,充分反应。当加入锌粉的质量为6.5g时,溶液质量最小;当加入锌粉的质量为13.0g时,恰好完全反应。下列是反应中的相关量随加入锌的质量变化的关系图,其中正确的是
A. | B. |
C. | D. |
6.天宫课堂中,航天员王亚平视频展示了在无容器材料实验柜中进行的“锆金属熔化与凝固”实验。金属锆具有抗腐蚀性强、熔点高、硬度大等特性,广泛用于航空航天、军工、原子能等领域。
(1)金属锆熔化属于______ (填“物理”或“化学”)变化。
(2)如图所示是锆元素在元素周期表中的信息,其中“40”是锆元素的原子序数,即它在元素周期表中的位置序号,也是锆原子的核电荷数(即质子数),由此可知锆原子的核外电子数为______ 。

(3)在850℃条件下,镁(Mg)与四氯化锆(ZrCl4)发生置换反应获得金属锆。该反应的化学方程式为:______ 。
(1)金属锆熔化属于
(2)如图所示是锆元素在元素周期表中的信息,其中“40”是锆元素的原子序数,即它在元素周期表中的位置序号,也是锆原子的核电荷数(即质子数),由此可知锆原子的核外电子数为

(3)在850℃条件下,镁(Mg)与四氯化锆(ZrCl4)发生置换反应获得金属锆。该反应的化学方程式为:
7.某维生素C泡腾片的主要成分如图甲所示。
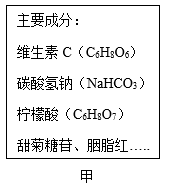
(1)维生素C由______ 种元素组成。
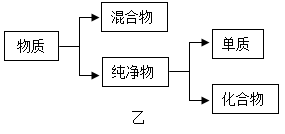
(2)按照如图乙的物质分类方法,该泡腾片属于______ 。
(3)该泡腾片放入水中,会立刻产生大量的气泡,其原因是:柠檬酸是一种酸,它和碳酸氢钠在水中会发生反应,生成能使澄清石灰水变浑浊的______ 气体。


(1)维生素C由
(2)按照如图乙的物质分类方法,该泡腾片属于
(3)该泡腾片放入水中,会立刻产生大量的气泡,其原因是:柠檬酸是一种酸,它和碳酸氢钠在水中会发生反应,生成能使澄清石灰水变浑浊的
8.某白色固体M可能由Na2CO3、Na2SO4、MgCl2、Ba(OH)2中的一种或几种物质组成。为确定其成分,小宁进行如图所示实验。
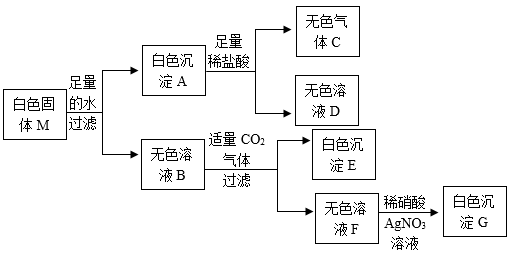
则:
(1)白色沉淀G的化学式为______ 。
(2)白色固体M的成分是______ 。

则:
(1)白色沉淀G的化学式为
(2)白色固体M的成分是
9.久置的镁带表面会有一层灰黑色固体。为了测量久置镁带中金属镁的质量分数,同学们提出了两种实验方法:
物理方法:取一定质量的镁带,用砂纸打磨,除尽表面的灰黑色固体,根据剩余固体质量计算金属镁的质量分数。
化学方法:取一定质量的镁带,与足量的稀硫酸反应,根据测得生成气体的体积计算金属镁的质量分数。
(1)经讨论,同学们否定了物理方法。理由是:打磨过程中______ 。
(2)常温常压下氢气密度已知,因此大家认为化学方法可行。
(老师提示:镁与稀硫酸反应放热;灰黑色固体除了氧化镁之外,还存在少量碱式碳酸镁【MgCO3•Mg(OH)2】,它与酸反应会产生CO2气体;碱石灰是CaO和NaOH的混合物)
同学们从下列装置中选择合适的装置,组装并进行实验。
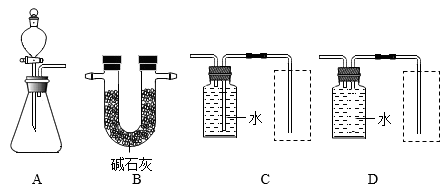
①图C、D虚线框内有一种测量体积的仪器(未画出),该仪器是______ 。
②完成该实验应选择的装置为______ (填字母)。
③结合实验方法和选择的装置分析,会造成实验结果不准确的是______ 。
A.加入稀硫酸不足,镁带有剩余
B.装置气密性不好
C.反应结束,立即读数
物理方法:取一定质量的镁带,用砂纸打磨,除尽表面的灰黑色固体,根据剩余固体质量计算金属镁的质量分数。
化学方法:取一定质量的镁带,与足量的稀硫酸反应,根据测得生成气体的体积计算金属镁的质量分数。
(1)经讨论,同学们否定了物理方法。理由是:打磨过程中
(2)常温常压下氢气密度已知,因此大家认为化学方法可行。
(老师提示:镁与稀硫酸反应放热;灰黑色固体除了氧化镁之外,还存在少量碱式碳酸镁【MgCO3•Mg(OH)2】,它与酸反应会产生CO2气体;碱石灰是CaO和NaOH的混合物)
同学们从下列装置中选择合适的装置,组装并进行实验。

①图C、D虚线框内有一种测量体积的仪器(未画出),该仪器是
②完成该实验应选择的装置为
③结合实验方法和选择的装置分析,会造成实验结果不准确的是
A.加入稀硫酸不足,镁带有剩余
B.装置气密性不好
C.反应结束,立即读数
10.“庄稼一枝花,全靠肥当家”。有一种新型化肥——硝酸铵钙,其有效成分为NH4NO3和Ca(NO3)2,进入土壤后,都成为可吸收的离子,不会引起土壤板结,且钙离子可提高农作物对病害的抵抗力。
小宁利用某品牌的硝酸铵钙化肥,进行以下实验:取化肥样品8.0g,与足量的NaOH固体充分混合,加热到固体质量不再减少,生成0.17g氨气(NH3)。把反应所得固体溶于适量水中,再加入足量的Na2CO3溶液充分反应,过滤得到沉淀和滤液,测得沉淀质量为4.0g。(已知:NH4NO3+NaOH NaNO3+NH3↑+H2O;化肥中的其它成分不含Ca、N元素,且不参加反应)
NaNO3+NH3↑+H2O;化肥中的其它成分不含Ca、N元素,且不参加反应)
(1)计算样品中NH4NO3的质量分数。
(2)计算滤液中NaNO3的质量。
小宁利用某品牌的硝酸铵钙化肥,进行以下实验:取化肥样品8.0g,与足量的NaOH固体充分混合,加热到固体质量不再减少,生成0.17g氨气(NH3)。把反应所得固体溶于适量水中,再加入足量的Na2CO3溶液充分反应,过滤得到沉淀和滤液,测得沉淀质量为4.0g。(已知:NH4NO3+NaOH
 NaNO3+NH3↑+H2O;化肥中的其它成分不含Ca、N元素,且不参加反应)
NaNO3+NH3↑+H2O;化肥中的其它成分不含Ca、N元素,且不参加反应)(1)计算样品中NH4NO3的质量分数。
(2)计算滤液中NaNO3的质量。
 搜索
搜索
 难度系数:0.85
难度系数:0.85  答案解析
答案解析
 有奖纠错
有奖纠错
