全一卷
1.化学使生活更美好。下列与生活相关的做法中,一定发生了化学变化的是
| A.用肥皂水区分出软水和硬水 | B.在云层中撒布干冰人工降雨 |
| C.用活性炭除去冰箱中的异味 | D.加热使某冷却变形合金复原 |
2.下列图示的实验操作,正确的是
A.滴加试剂 | B.稀释浓硫酸 |
C.读取液体体积 | D.移走蒸发皿 |
3.化学既需要“见微知著”,又需要“见著知微”。下列分析不合理的是
| 选项 | 宏观现象辨识 | 微观原因探析 |
| A | 墙内开花墙外香 | 分子在不停地运动 |
| B | 很多果汁有酸味 | 这些果汁中含有氢离子 |
| C | 冰融化后体积变小 | 分子间间隔可以改变 |
| D | C60与C18的性状不同 | 分子是保持物质性质的最小粒子 |
| A.A | B.B | C.C | D.D |
4.新冠疫情当前在一些国家和地区仍呈失控之势,消毒能有效阻止病毒传播。“84消毒液”(含有NaClO)、二氧化氯(ClO2)都是常用的含氯消毒剂,下列有关NaClO、ClO2的叙述正确的是
| A.两物质中Cl的化合价相同 | B.ClO2中含有O2 |
| C.Cl核外最外层电子数为7 | D.NaClO含氯率更高 |
5.在Cu(NO3)2、Mg(NO3)2和AgNO3混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中滴加稀硫酸时有气泡产生。滤渣中没有
| A.Cu | B.Mg | C.Ag | D.Fe |
6.某溶液中可能含有HCl、CuCl2、Na2SO4中的一种或几种溶质,向一定量该溶液中不断滴加Ba(OH)2溶液,产生沉淀质量与所加Ba(OH)2溶液质量之间的关系如图所示,下列判断错误的是


| A.原溶液中一定不含Na2SO4 | B.原溶液中一定含有HCl |
| C.b点溶液中只含一种溶质 | D.对应溶液的pH:a<b=c |
7.化学用语是学习化学的重要工具。按要求用化学用语填空:
地壳中含量最多的金属元素是________ 、其原子结构示意图为_____ ,它与地壳中含量最多的非金属元素组成的化合物为______ ,在该化合物中金属元素的化合价为_______ 、阳离子符号为________ 。
地壳中含量最多的金属元素是
8.化学与生产生活密切相关。回答下列问题:
(1)我国所产棉花纤维柔长、洁白有光,棉花属于_______ (填“天然”或“合成”)纤维。熔喷布是制作防疫口罩的关键材料,它的主要成分为聚丙烯【(C3H6)n】,聚丙烯中H的质量分数为______ 。
(2)袁隆平院士的研究团队曾在我国高盐碱地区试种“海水稻”,高盐碱地区土壤的pH超过8.5,土壤pH越大、其碱性越________ (填“强”或“弱”);“海水稻”大米提供的主要营养物质是__________ 。化肥对提高农作物的产量具有重要作用,下列化肥中属于复合肥的是______ (填选项序号)。
a. NH4NO3 b. Ca3(PO4)2 c. KNO3 d. KCl
(3)垃圾分类,意义重大。空易拉罐是________ (填选项序号)。
a.厨余垃圾 b.可回收垃圾 c.有害垃圾 d.其他垃圾
(1)我国所产棉花纤维柔长、洁白有光,棉花属于
(2)袁隆平院士的研究团队曾在我国高盐碱地区试种“海水稻”,高盐碱地区土壤的pH超过8.5,土壤pH越大、其碱性越
a. NH4NO3 b. Ca3(PO4)2 c. KNO3 d. KCl
(3)垃圾分类,意义重大。空易拉罐是
a.厨余垃圾 b.可回收垃圾 c.有害垃圾 d.其他垃圾
9.硝酸钾、氯化铵、氯化钠的溶解度曲线如图所示。

回答下列问题:
(1)20℃时,三种物质中溶解度最大的是_______ (填化学式)。
(2)70℃时,氯化铵饱和溶液中溶质与溶剂的质量之比为________ (填最简单整数比)。
(3)将t1℃时的三种物质饱和溶液均升温至t2℃,所得溶液中溶质的质量分数最小的是_______ (填化学式)。

回答下列问题:
(1)20℃时,三种物质中溶解度最大的是
(2)70℃时,氯化铵饱和溶液中溶质与溶剂的质量之比为
(3)将t1℃时的三种物质饱和溶液均升温至t2℃,所得溶液中溶质的质量分数最小的是
10.高纯硅是制造芯片的基础材料,工业上制取高纯硅过程中的一个反应的微观示意图如下:

回答下列问题:
(1)该反应的化学方程式为________ 。
(2)在化学反应前后,可能发生了改变的是______ (填选项序号)。
a.原子数目 b.分子数目 c.元素种类 d.物质的总质量

回答下列问题:
(1)该反应的化学方程式为
(2)在化学反应前后,可能发生了改变的是
a.原子数目 b.分子数目 c.元素种类 d.物质的总质量
11.如图是以物质类别为横坐标、碳的化合价为纵坐标制成的碳元素“价类二维图”。
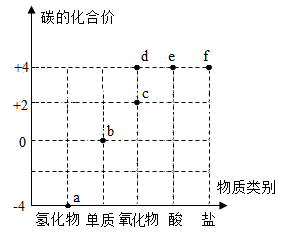
回答下列问题:
(1)为实现“碳中和”,科学家们正在研究将d点对应物质与某单质反应转化为a点对应物质(还生成了其他物质),该单质是___________ (填化学式)。
(2)b点对应物质有多种,我国晋代炼丹家葛洪在他所著的《抱朴子•内篇》中对其中一种物质有这样的描述“……生水底石上,如钟乳状,体似紫石英,可以刻玉,人没水取之,虽铁椎击之亦不能伤”,文中描述的物质是___________ (填名称)。
(3)c、d点对应物质在一定条件下的转化关系如下:c点对应物质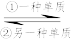 d点对应物质;反应①的化学方程式为
d点对应物质;反应①的化学方程式为 ___________ ,反应②的基本反应类型为 ___________ 。
(4)设计一个简单实验,证明d点对应物质可变为e点对应物质___________ 。
(5)f点对应物质有多种,其中___________ (填化学式)是焙制糕点所用的发酵粉的主要成分之一、

回答下列问题:
(1)为实现“碳中和”,科学家们正在研究将d点对应物质与某单质反应转化为a点对应物质(还生成了其他物质),该单质是
(2)b点对应物质有多种,我国晋代炼丹家葛洪在他所著的《抱朴子•内篇》中对其中一种物质有这样的描述“……生水底石上,如钟乳状,体似紫石英,可以刻玉,人没水取之,虽铁椎击之亦不能伤”,文中描述的物质是
(3)c、d点对应物质在一定条件下的转化关系如下:c点对应物质
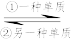 d点对应物质;反应①的化学方程式为
d点对应物质;反应①的化学方程式为 (4)设计一个简单实验,证明d点对应物质可变为e点对应物质
(5)f点对应物质有多种,其中
12.实验室常用下列A、B、C装置制取气体,D、E、F装置收集气体。
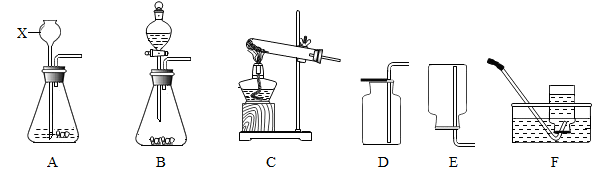
回答下列问题:
(1)A装置中仪器X的名称是___________ 。
(2)若用B装置制取氧气,反应的化学方程式为___________ 。在D、E中需选择 ___________ 集氧气,选择的依据是 ___________ 。
(3)实验室常以氯酸钾、二氧化锰为原料,用C装置制取、F装置收集氧气。实验前需检查装置的气密性:连接装置C、F,微热C中试管,若F中产生气泡、且恢复常温后玻璃管内水面___________ 水槽的水面,就证明装置气密性良好。将反应后剩余固体溶解、过滤、洗净、干燥后又得到二氧化锰固体,其质量与反应前相比 ___________ (填“增大”“减小”或“不变”)。
(4)若以高锰酸钾为原料、用C装置制取氧气,需要在___________ 塞一团棉花。

回答下列问题:
(1)A装置中仪器X的名称是
(2)若用B装置制取氧气,反应的化学方程式为
(3)实验室常以氯酸钾、二氧化锰为原料,用C装置制取、F装置收集氧气。实验前需检查装置的气密性:连接装置C、F,微热C中试管,若F中产生气泡、且恢复常温后玻璃管内水面
(4)若以高锰酸钾为原料、用C装置制取氧气,需要在
13.2020年我国仅用10天的时间就建造起了武汉火神山医院,其建材中使用了HDPE膜,它具有良好的抗冲击性和防潮性。某项目式学习小组对HDPE膜的组成元素产生浓厚兴趣,进行了以下探究:
【查阅资料】①碱石灰的主要成是NaOH和CaO;②HDPE膜不含氮元素。
【提出问题】HDPE膜由什么元素组成?
【进行实验】称取2.8 g HDPE膜,按下图组装仪器,先通入氮气,再点燃酒精灯、通入一定量氧气使HDPE膜燃尽,实验中装置B、C、D、E、F对能吸收的气体均完全吸收。

【记录数据】
【讨论交流】
(1)装置B质量增加,说明HDPE膜燃烧产物中有______ (填化学式);装置C中铜丝表面的黑色固体变红,该反应的化学方程式为________ 。
(2)根据实验数据和现象判断:HDPE膜中一定含有_______ 、______ (填元素符号)元素。
(3)装置F的作用是_________ 。
(4)根据实验数据判断:HDPE膜中_______ (填“含”或“不含”)氧元素。
【反思评价】
(5)每年的6月5日为世界环境日。化学实验中如果产生了尾气,需对尾气进行处理,其目的是_______ 。
【查阅资料】①碱石灰的主要成是NaOH和CaO;②HDPE膜不含氮元素。
【提出问题】HDPE膜由什么元素组成?
【进行实验】称取2.8 g HDPE膜,按下图组装仪器,先通入氮气,再点燃酒精灯、通入一定量氧气使HDPE膜燃尽,实验中装置B、C、D、E、F对能吸收的气体均完全吸收。

【记录数据】
| B装置总质量/g | D装置总质量/g | E装置总质量/g | |
| 点燃酒精灯前 | 120 | 120 | 120 |
| 实验结束后 | 123.6 | 120 | 128.8 |
【讨论交流】
(1)装置B质量增加,说明HDPE膜燃烧产物中有
(2)根据实验数据和现象判断:HDPE膜中一定含有
(3)装置F的作用是
(4)根据实验数据判断:HDPE膜中
【反思评价】
(5)每年的6月5日为世界环境日。化学实验中如果产生了尾气,需对尾气进行处理,其目的是
14.化学实验室有一瓶标签损坏的Na2CO3溶液,为测定其溶质的质量分数,甲、乙实验小组均取20g该溶液与20g稀盐酸(过量)充分反应。甲组将反应所得的盐全部转变为固体,称得其质量为2.34g;乙组测得反应后混合溶液的质量为39.12g。
回答下列问题:
(1)比较两组实验方案,乙组的优点是_______ ,可能存在的问题是_________ 。
(2)任选一组的实验数据,计算Na2CO3溶液中溶质的质量分数。(写出计算过程,如果选择两组数据计算,按第一个解答计分)
回答下列问题:
(1)比较两组实验方案,乙组的优点是
(2)任选一组的实验数据,计算Na2CO3溶液中溶质的质量分数。(写出计算过程,如果选择两组数据计算,按第一个解答计分)
 搜索
搜索
 难度系数:0.85
难度系数:0.85  答案解析
答案解析
 有奖纠错
有奖纠错
