全一卷
1.物理变化、化学变化是生活中的常见现象,下列属于化学变化的是( )
| A.铁水铸成锅 |
| B.纸张燃烧 |
| C.水蒸气变成水 |
| D.汽油挥发 |
2.生活中的下列物质属于纯净物的是( )
| A.酱油 | B.豆浆 | C.海水 | D.氧气 |
3.化学是一门以实验为基础的科学,实验室用高锰酸钾制氧气的实验中,下列仪器不需要使用的是( )
| A.玻璃棒 | B.大试管 | C.铁架台 | D.单孔塞 |
4.下列化学反应及变化中叙述正确的是( )
| A.NO2中N元素的化合价是+3价 |
B. 该反应类型为置换反应 该反应类型为置换反应 |
| C.氧气的化学性质很活泼,在常温下能与所有物质发生化学反应 |
D.稀硫酸与氢氧化钠溶液反应的化学方程式为 |
5.化学就在我们身边,下列说法正确的是( )
| A.pH值小于7的降雨称为酸雨 |
| B.二氧化碳极易与血红蛋白结合,造成生物体内缺氧 |
| C.空气是一种混合物,空气的成分按体积计氮气约占78% |
| D.溶液在生活中应用广泛,均一、稳定的液体都是溶液 |
6.下列有关物质构成的说法中正确的是( )
| A.分子是由原子构成的 |
| B.分子是化学变化中的最小粒子 |
| C.相同原子无法构成不同的分子 |
| D.元素周期表共有7个纵行,18个横行 |
7.下列叙述错误的是( )
| A.硫在氧气中燃烧发出蓝紫色火焰,生成二氧化硫气体 |
| B.实验室丢失标签的KCl、NaOH、CuSO4三瓶溶液,不用加其他试剂就可相互鉴别 |
| C.不慎将浓硫酸沾到皮肤上,立即用大量水冲洗,再涂上3%﹣5%的碳酸氢钠溶液 |
| D.密闭容器中,3.4g H2O2完全分解,生成物的质量分别是:2.0g H2O,1.4g O2 |
8.下列物质的名称、俗称与用途对应正确的是( )
| | 物质名称 | 俗称 | 用途 |
| A | 碳酸钠 | 火碱 | 制造玻璃 |
| B | 碳酸氢钠 | 苏打 | 焙制糕点 |
| C | 氢氧化钙 | 消石灰 | 改良酸性土壤 |
| D | 甲醛溶液 | 福尔马林 | 长期保鲜食品 |
| A.A | B.B | C.C | D.D |
9.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
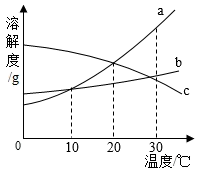

| A.a、b两种物质的溶解度相等 |
| B.a、b、c三种物质的溶解度大小顺序为a>b>c |
| C.从0℃到30℃时,随着温度的升高,c物质的溶解度变化最小 |
| D.温度从10℃到20℃时,a、b两种物质的溶解度都在增大,其中a物质的溶解度受温度影响较大 |
10.用化学符号或化学式填空:
(1)2个钾原子_____。
(2)3个氖气分子_____。
(3)甲烷的化学式_____。
(4)氢氧化铜中的阳离子_____。
(1)2个钾原子_____。
(2)3个氖气分子_____。
(3)甲烷的化学式_____。
(4)氢氧化铜中的阳离子_____。
11.食醋、KNO3、加碘食盐、尿素[CO (NH2)2]、棉花、干冰等是生活中常见物质,请用所学的化学知识选择上述物质完成下列问题:
(1)能有效预防大脖子病的是_____ 。
(2)能使石蕊溶液变红的是_____ 。
(3)属于天然高分子化合物的是_____ 。
(4)用于人工降雨的物质是_____ 。
(5)化肥对提高农作物的产量具有重要作用,属于复合肥料的是_____ 。
(1)能有效预防大脖子病的是
(2)能使石蕊溶液变红的是
(3)属于天然高分子化合物的是
(4)用于人工降雨的物质是
(5)化肥对提高农作物的产量具有重要作用,属于复合肥料的是
12.水、燃烧与我们生活息息相关。
(1)水是生命之源,生活中常用_____ 的方法降低水的硬度。
(2)燃烧与人类的生活以及社会的发展有着密切的联系,通常情况下,燃烧需要三个条件:氧气(或空气)、可燃物、_____ 。熄灭酒精灯,用灯帽盖的方法,采用的原理是_____ 。
(1)水是生命之源,生活中常用
(2)燃烧与人类的生活以及社会的发展有着密切的联系,通常情况下,燃烧需要三个条件:氧气(或空气)、可燃物、
13.请用化学知识回答下列问题。
(1)铜仁市的锰资源非常丰富,锰及锰的化合物应用广泛,实验室用氯酸钾和二氧化锰混合制取氧气,二氧化锰作用是_____。
(2)金刚石、石墨和C60都是由碳元素组成的单质,但它们的物理性质差异较大,石墨具有_____可制成电极。
(3)钢铁在生活中应用广泛,在潮湿的空气中铁制品容易生锈(铁锈的主要成分是Fe2O3),用稀硫酸除铁锈的化学方程式为_____。
(4)金属及金属材科在生产生活中有广泛的应用,请根据相关信息回答问题。
①现有铁、铜、锌三种金属,请选择一种试剂_____(填化学式),通过实验证明它们金属活动性的强弱。
②金属钠非常活泼,在自然界以化合物的形式存在,近年来对钠电池的研究也取得了较大进展。工业上常用电解熔融状态的氯化钠制取单质钠,并产生氯气(Cl2),请写出该反应的化学方程式_____(该反应与电解水类似)。
(1)铜仁市的锰资源非常丰富,锰及锰的化合物应用广泛,实验室用氯酸钾和二氧化锰混合制取氧气,二氧化锰作用是_____。
(2)金刚石、石墨和C60都是由碳元素组成的单质,但它们的物理性质差异较大,石墨具有_____可制成电极。
(3)钢铁在生活中应用广泛,在潮湿的空气中铁制品容易生锈(铁锈的主要成分是Fe2O3),用稀硫酸除铁锈的化学方程式为_____。
(4)金属及金属材科在生产生活中有广泛的应用,请根据相关信息回答问题。
①现有铁、铜、锌三种金属,请选择一种试剂_____(填化学式),通过实验证明它们金属活动性的强弱。
②金属钠非常活泼,在自然界以化合物的形式存在,近年来对钠电池的研究也取得了较大进展。工业上常用电解熔融状态的氯化钠制取单质钠,并产生氯气(Cl2),请写出该反应的化学方程式_____(该反应与电解水类似)。
14.今年新型冠状病毒疫情肆虐全球,我国在抗击疫情方面充分体现了大国担当,通过全国人民共同努力有效控制住了疫情的发展。
(1)疫情期间,某食品公司向医院捐赠了一批“即热米饭”,该“即热米饭”用生石灰和水的反应作为热源,请写出化学方程式_____,在饮食搭配中一定要注意营养均衡,该“即热米饭”料包中含有米饭、胡萝卜、牛肉、青菜等,其中主要含蛋白质的是_____。
(2)在日常生活中要养成良好的生活方式,勤洗手能有效保护自己,减少病毒和细菌的入侵,下列可用于手部消毒的物质为_____。
A 浓硫酸
B 酒精
C 洁厕灵
D 84消毒液
(1)疫情期间,某食品公司向医院捐赠了一批“即热米饭”,该“即热米饭”用生石灰和水的反应作为热源,请写出化学方程式_____,在饮食搭配中一定要注意营养均衡,该“即热米饭”料包中含有米饭、胡萝卜、牛肉、青菜等,其中主要含蛋白质的是_____。
(2)在日常生活中要养成良好的生活方式,勤洗手能有效保护自己,减少病毒和细菌的入侵,下列可用于手部消毒的物质为_____。
A 浓硫酸
B 酒精
C 洁厕灵
D 84消毒液
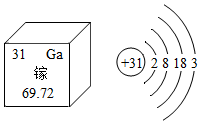
15.金属镓的性质与铝相似,镓在元素周期表中的相关信息及原子结构示意图如图,请回答下列问题:
(1)镓元素的相对原子质量_____ 。
(2)镓原子的最外层电子数为_____ 个。
(3)根据原子结构示意图,可知镓原子的最外层电子在反应中容易失去,请写出金属镓与稀硫酸反应的化学方程式_____ 。
(1)镓元素的相对原子质量
(2)镓原子的最外层电子数为
(3)根据原子结构示意图,可知镓原子的最外层电子在反应中容易失去,请写出金属镓与稀硫酸反应的化学方程式

16.根据下列图示实验装置。回答有关问题。
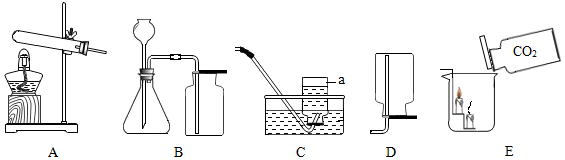
(1)写出标有字母a的仪器名称_____ 。
(2)实验室用大理石制取CO2的反应原理_____ (用化学方程式表示),选择_____ (填字母)装置制取二氧化碳。
(3)从图E观察到的现象说明CO2具有性质是_____ ,写出检验CO2气体的方法_____ (用化学方程式表示)。
(4)写出实验室选用A装置制取氧气的反应方程式_____ ,实验室要得到比较纯净的氧气通常选用_____ (填字母)装置收集。

(1)写出标有字母a的仪器名称
(2)实验室用大理石制取CO2的反应原理
(3)从图E观察到的现象说明CO2具有性质是
(4)写出实验室选用A装置制取氧气的反应方程式
17.酸碱盐在工农业生产和生活中应用广泛,请用所学化学知识回答问题。
(1)日常生活中有以下常见物质:白醋、纯碱、苛性钠、小苏打、硫酸铵,其中属于碱的是_____ (填上述物质)。将少量无色酚酞溶液滴加到碱溶液中,溶液变_____ 。
(2)如饮食不当,胃会分泌出大量胃酸,服用含有下列哪种物质的药物可以中和过多胃酸,写出反应的化学方程式_____ 。
A NaOH
B Na2CO3
C Al(OH)3
(3)某氯化钠样品中,可能含有杂质:BaCl2、MgCl2、Na2SO4中的一种或几种,某校课外化学兴趣小组的同学进行实验探究杂质成分,探究过程如图(已知氢氧化镁难溶于水):
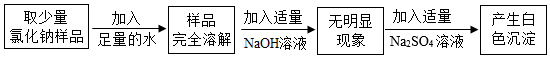
根据以上实验信息,用_____ 操作方法,可将上述实验过程中产生的白色沉淀与溶液分离,加入适量NaOH溶液的目的是_____ ,写出杂质与Na2SO4溶液反应的化学方程式_____ 。
(1)日常生活中有以下常见物质:白醋、纯碱、苛性钠、小苏打、硫酸铵,其中属于碱的是
(2)如饮食不当,胃会分泌出大量胃酸,服用含有下列哪种物质的药物可以中和过多胃酸,写出反应的化学方程式
A NaOH
B Na2CO3
C Al(OH)3
(3)某氯化钠样品中,可能含有杂质:BaCl2、MgCl2、Na2SO4中的一种或几种,某校课外化学兴趣小组的同学进行实验探究杂质成分,探究过程如图(已知氢氧化镁难溶于水):
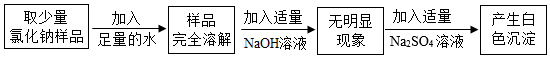
根据以上实验信息,用
18.铜粉中混有少量的铁粉,为了除去铁粉,某校兴趣小组同学,取该铜粉20g于烧杯中,然后等量分5次加入未知质量分数的某强酸(W)溶液,充分反应后所得数据如下表,请根据相关知识和图表信息回答下列问题。
(1)写出你所选择酸(W)的化学式 。
(2)铜粉中混有铁粉的质量是 。
(3)计算你选择酸(W)的质量分数(写出计算过程)。
| 项目 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入W溶液的质量/g | 5 | 5 | 5 | 5 | 5 |
| 每次产生气体的质量/g | 0.01 | 0.01 | 0.01 | 0.005 | 0 |
(1)写出你所选择酸(W)的化学式 。
(2)铜粉中混有铁粉的质量是 。
(3)计算你选择酸(W)的质量分数(写出计算过程)。
 搜索
搜索
 难度系数:0.94
难度系数:0.94  答案解析
答案解析
 有奖纠错
有奖纠错
