全一卷
1.古诗词是中华民族的文化瑰宝,下列古诗词中对划线对象变化的描述属于化学变化的是
| A.一味黑时犹有骨,十分红处便成灰。([清]徐宗干《咏炭》) |
| B.河上姹女(水银),灵而最神,得火则飞,不见埃尘。([汉]魏伯阳《参同契》) |
| C.臣心一片磁针石,不指南方不肯休。([宋]文天祥《扬子江》) |
| D.落红(落花)不是无情物,化作春泥更护花。([清]龚自珍《己亥杂诗》) |
2.中药的煎制直接关系到其疗效。下列制备中草药汤剂的步骤中,与过滤操作类似的是
A. 浸泡 浸泡 |
B. 煎制 煎制 |
C. 滗汤 滗汤 |
D. 灌装 灌装 |
3.2017 年 1 月 26 日美国《科学》杂志报道,哈佛大学实验室对液氢样本施加 4.95×10 11Pa 压力,成功制造出了金属氢,这是一种以氢离子和自由电子为基本单位构成的晶体。关于金属氢的推测错误的是
| A.与氢气互为同素异形体 |
| B.制造金属氢过程属于化学变化 |
| C.可能具有良好的导电性 |
| D.摩尔质量与氢气相同 |
4.“酸雨”成为当今主要的环境问题之一,雨水在未被污染的大气中原本应该呈
| A.弱酸性 | B.中性 | C.弱碱性 | D.强酸性 |
5.下列实验操作中,与其他三项的目的不属于同一类的是( )
| A.点燃甲烷、一氧化碳等可燃性气体前,先检验气体的纯度 |
| B.做中和反应实验时,先在碱溶液中滴入1~2滴酚酞溶液 |
| C.在进行铁丝燃烧实验前,先向充满氧气的集气瓶加入一层细沙 |
| D.在使用氢气还原氧化铜时,先向硬质玻璃管中通入氢气 |
6.质量相等的石墨和足球烯(化学式C60)所含原子数
| A.前者多 | B.相等 | C.后者多 | D.无法确定 |
7.有一瓶配制好的 NaCl 稀溶液,在实验室里敞口放置数天后外观无明显变化,关于它的说法正确的是
| A.瓶底附近的溶液较浓 |
| B.瓶口附近的溶液较浓 |
| C.溶质的质量分数不变 |
| D.瓶内的溶液中各部分浓度相同 |
8.下图是表示物质微粒的示意图,图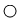 和
和 两小球分别表示两种不同元素的原子,其中表示混合物的是
两小球分别表示两种不同元素的原子,其中表示混合物的是
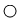 和
和 两小球分别表示两种不同元素的原子,其中表示混合物的是
两小球分别表示两种不同元素的原子,其中表示混合物的是A. | B. | C. | D. |
9.英国科学家法拉第曾用蜡烛(主要成分石蜡)做过一个有趣的“母子火焰”实验,如图所示。据此实验,下列有关分析中正确的是( )
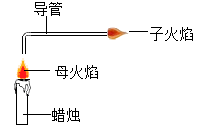

| A.这一现象说明石蜡的熔点较低 |
| B.要使实验成功,导管不宜过长 |
| C.子火焰中被燃烧的物质是石蜡分解产生的氢气 |
| D.导管的一端要插入母火焰的中心部位是因为该处氧气充足 |
10.X 是一种白色固体。加热 X 时,会产生另一种固体 Y 和气体 Z。已知 Y 属于纯净物,气体 Z 可以通过碳与氧气反应得到。从上述信息中可以得出的结论是
| A.X、Y、Z 一定都属于化合物 |
| B.X、Z 中一定都含有碳元素 |
| C.X、Y、Z 中一定都含有氧元素 |
| D.X、Y 中一定含有金属元素 |
11. 溶液的酸碱性也会影响难溶物的溶解性,下列难溶物在一定量水中的溶解量会随pH降低而增加的是
| A.SiO2 | B.AgCl | C.BaSO4 | D.Mg(OH)2 |
12.某+3 价金属的氧化物 xg 完全还原后,得到 yg 该金属。则该金属的摩尔质量数值可表示为
A. | B. | C. | D. |
13.如图所示装置具有多种用途,下列实验均要使用该装置(不改变瓶口朝向),其中 x 为气体或水入口的是
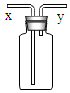

| A.排空气法收集H2 |
| B.瓶中装有 NaOH 溶液,除去H2中少量CO2 |
| C.瓶中装有O2,加水以取用瓶内储存气体 |
| D.瓶中装满水,用排水集气法收集O2 |
14.如图所示,25℃下向某密闭容器中充入一定量的CO2与水,充分溶解后保持温度不变,打开活塞排走一半体积的水,则剩余水中CO2的浓度将
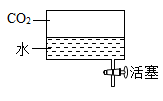

| A.上升 | B.下降 | C.不变 | D.无法确定 |
15.某化合物MX6分子呈正八面体形式(如图所示)。由于六个 X 原子与 M 的连接完全对称,因此将任意一个 X 用 Y 原子替换,均只能得到一种结构的MX5Y分子,按此思路, 若将其中任意两个 X 原子用 Y 原子替换,则得到的化学式为MX4Y2的分子
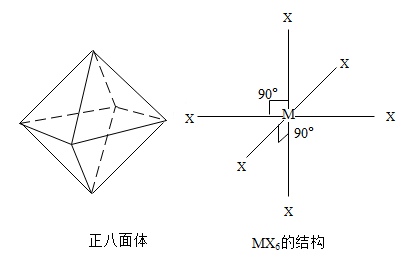

| A.只有 1 种结构 |
| B.存在 2 种不同结构 |
| C.存在 3 种不同结构 |
| D.存在 4 种不同结构 |
16.下列各组图像可能描述同一个反应的是
A. |
B. |
C. |
D. |
17.各种化学元素在不同自然物质体系中含量(按质量分数计)不同,按要求写出对应的元素名称:
(1)地壳中含量最高的金属元素:________;
(2)大气中含量最高的元素:_;
(3)除氢、氧外,海水中含量最高的元素:_;
(4)人体中含量最高的金属元素:_;
(5)宇宙中含量最高的元素:_。
(1)地壳中含量最高的金属元素:________;
(2)大气中含量最高的元素:_;
(3)除氢、氧外,海水中含量最高的元素:_;
(4)人体中含量最高的金属元素:_;
(5)宇宙中含量最高的元素:_。
18.汽车排出的废气中,常含有 CO、NO 和碳氢化合物(以 CxHy 表示)等,它们会污染环境,为防止此类污染,可采用催化转换器,将这些化合物转变成无害的物质。方法是: 把汽车气缸排出的废气送入第一个转换器,用 CO 还原 NO,再将排出的气体与过量空气一起,送入第二个转换器,使剩余的 CO 和 CxHy 充分氧化。写出两个转换器中涉及反应的化学方程式:
(1)第一个转换器:_ 。
(2)第二个转换器:_ 。
(1)第一个转换器:
(2)第二个转换器:
19.在图中的烧杯中盛有65℃的热水,杯底放有一小粒足够量的白磷,然后将一支有刻度的空试管垂直插入烧杯中,试管口罩住白磷。(已知白磷熔点 44℃,着火点为 40℃)。
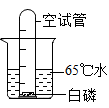
(1)写出实验过程中发生的现象_ 。
(2)该实验说明了_ 。

(1)写出实验过程中发生的现象
(2)该实验说明了
20.如图是甲、乙、丙三种物质的溶解度曲线。
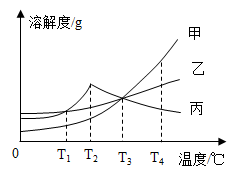
(1)三种物质溶解度关系为甲<乙<丙时的温度为 T℃,则 T 的取值范围为_________ 。
(2)现有含有少量甲的乙固体,若要通过结晶法进行提纯(甲与乙不发生反应),现有下列实验步骤可供选择:
①取一定质量水将固体溶解
②充分冷却后过滤
③趁热过滤
④加热蒸发至有大部分晶体析出
⑤加热蒸发至溶液接近饱和
⑥停止加热,用余热将溶液蒸干
⑦用少量水洗涤晶体并烘干
合理的操作顺序为:__________ (按顺序选填编号)
(3)T4℃时,取相同质量的甲、乙、丙三种饱和溶液,恒温蒸发一定质量的水(析出晶体均不含结晶水),剩余溶液质量大小关系为:甲=乙<丙。则析出晶体质量大小关系为______________ 。
(4)已知丙溶液在T2℃以下析出晶体含有结晶水,在T2℃以上析出的晶体不含结晶水, 现将一定质量T1℃时丙的饱和溶液冷却至 Ta℃或升高至Tb℃时,析出晶体质量相等,则三种温度下丙(指无水物)的溶解度 S1、Sa、Sb 的大小关系为:__________________ (选 填编号)。
a S1>Sa>Sb
b S1>Sa=Sb
c S1>Sb>Sa
d Sb>S1>Sa

(1)三种物质溶解度关系为甲<乙<丙时的温度为 T℃,则 T 的取值范围为
(2)现有含有少量甲的乙固体,若要通过结晶法进行提纯(甲与乙不发生反应),现有下列实验步骤可供选择:
①取一定质量水将固体溶解
②充分冷却后过滤
③趁热过滤
④加热蒸发至有大部分晶体析出
⑤加热蒸发至溶液接近饱和
⑥停止加热,用余热将溶液蒸干
⑦用少量水洗涤晶体并烘干
合理的操作顺序为:
(3)T4℃时,取相同质量的甲、乙、丙三种饱和溶液,恒温蒸发一定质量的水(析出晶体均不含结晶水),剩余溶液质量大小关系为:甲=乙<丙。则析出晶体质量大小关系为
(4)已知丙溶液在T2℃以下析出晶体含有结晶水,在T2℃以上析出的晶体不含结晶水, 现将一定质量T1℃时丙的饱和溶液冷却至 Ta℃或升高至Tb℃时,析出晶体质量相等,则三种温度下丙(指无水物)的溶解度 S1、Sa、Sb 的大小关系为:
a S1>Sa>Sb
b S1>Sa=Sb
c S1>Sb>Sa
d Sb>S1>Sa
21.高炉炼铁所需的原料有铁矿石、焦炭、石灰石等,其过程可用下图简要表示:
已知气体①、气体②和固体③均属于氧化物。
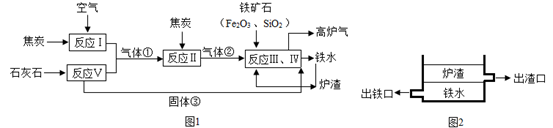
(1)气体②的化学式为_____ 。根据氧化物的性质推测炉渣的主要成分为_____ (填化学式)。
(2)炼铁高炉底部通过不同高度的出口分离铁水与炉渣(如图2所示)。能实现渣铁分离的原因是是因为炉渣具有_____ 、_____ 的性质。
(3)反应Ⅰ~Ⅴ中属于化合反应的有_____ 个,属于分解反应的有_____ 个,属于置换反应的有_____ 个。
(4)高炉气体中含有多种成分,其中含量最高(占55%~60%)的是_____ (填化学式),此外还含有25~30%的可燃性气体_____ (填化学式),以及9~12%左右的_____ (填化学式)。
已知气体①、气体②和固体③均属于氧化物。

(1)气体②的化学式为
(2)炼铁高炉底部通过不同高度的出口分离铁水与炉渣(如图2所示)。能实现渣铁分离的原因是是因为炉渣具有
(3)反应Ⅰ~Ⅴ中属于化合反应的有
(4)高炉气体中含有多种成分,其中含量最高(占55%~60%)的是
22.某同学研究亚硫酸钠(化学式为 Na2SO3)热分解反应时,作了两种假设:
假设一:它按 CaCO3受热方式来分解。
假设二:它按 KClO3受热分解方式来分解。
(1)假设一对应的化学方程式是________。确认假设二是否成立的简单实验操作是_____。
(2)该同学将取一定质量的样品置于坩埚中充分灼烧,发现最终得到固体质量较原样品质量增加了大约 12.7%。据此他认为_(选填编号)。
a 假设一成立
b 假设二成立
c 两种假设均不成立
固体质量增加可能的原因是________。
(3)在查阅资料后,该同学再次进行了实验。他将一定质量样品置于密闭真空容器中充分加热,最终得到固体质量与原样品相同。但进一步分析表明,该固体组成为两种新的钠盐,其物质的量之比为 1:3。请写出相应的化学方程式_。
(4)该同学想要进一步探究次氯酸钠(化学式 NaClO)的分解反应。他查阅资料后,得知NaClO 有多种热分解方式(每种分解方式的产物仅有两种)。若其中一种产物为 NaCl,则另一种产物可能是:________(选填编号)。
a Cl2
b O2
c Na2O
d NaClO3
假设一:它按 CaCO3受热方式来分解。
假设二:它按 KClO3受热分解方式来分解。
(1)假设一对应的化学方程式是________。确认假设二是否成立的简单实验操作是_____。
(2)该同学将取一定质量的样品置于坩埚中充分灼烧,发现最终得到固体质量较原样品质量增加了大约 12.7%。据此他认为_(选填编号)。
a 假设一成立
b 假设二成立
c 两种假设均不成立
固体质量增加可能的原因是________。
(3)在查阅资料后,该同学再次进行了实验。他将一定质量样品置于密闭真空容器中充分加热,最终得到固体质量与原样品相同。但进一步分析表明,该固体组成为两种新的钠盐,其物质的量之比为 1:3。请写出相应的化学方程式_。
(4)该同学想要进一步探究次氯酸钠(化学式 NaClO)的分解反应。他查阅资料后,得知NaClO 有多种热分解方式(每种分解方式的产物仅有两种)。若其中一种产物为 NaCl,则另一种产物可能是:________(选填编号)。
a Cl2
b O2
c Na2O
d NaClO3
23.化合物中某一种元素的原子短缺可形成非整比化合物,这类化合物中各类原子的相对数目不能用简单整数比表示,如Fe0.9O、PbO1.9等。非整比化合物是新型的功能材料,具有很大的科技价值。
(1)PbO1.9中铅元素具有+2、+4 两种价态,其中+4 价铅占铅总量的_______ 。
(2)如图所示,Fe0.9O可用于CO2的综合利用。

①请写出该转化的两个优点:___________ 、__________ 。
②若用1mol Fe0.9O与足量的CO2完全反应可生成_ g C(碳)。
(1)PbO1.9中铅元素具有+2、+4 两种价态,其中+4 价铅占铅总量的
(2)如图所示,Fe0.9O可用于CO2的综合利用。

①请写出该转化的两个优点:
②若用1mol Fe0.9O与足量的CO2完全反应可生成
24.已知 CuS、Cu2S 粉末的颜色和 CuO 相似,且都不溶解于水。在空气中煅烧时,CuS 和Cu2S 都转化成 CuO 和 SO2。
(1)请写出 CuS、Cu2S 在空气中煅烧时发生反应的化学方程式:________、________。
(2)根据叙述,设计一个不用其他化学试剂鉴别 CuO、CuS、Cu2S三种粉末的实验方案(写明步骤与结论)________。
(1)请写出 CuS、Cu2S 在空气中煅烧时发生反应的化学方程式:________、________。
(2)根据叙述,设计一个不用其他化学试剂鉴别 CuO、CuS、Cu2S三种粉末的实验方案(写明步骤与结论)________。
25.半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2 和H2O(g)。半水煤气经过下列步骤转化为合成氨的原料N2和H2。
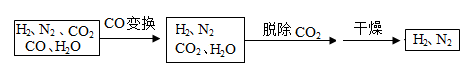
(1)在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应实现了 CO 变换,其化学方程式为:________ 。
(2)吸收法是脱除CO2的方法之一。已知:
若选择Na2CO3溶液作吸收液,其优点是_ ;缺点是_ 。如果选择K2CO3溶液作吸收液,用某种方法可以降低成本,写出这种方法涉及的化学方程式:_ 。
(3)将一定体积半水煤气依次通过装置Ⅰ~Ⅴ(最后通入氮气确保反应、吸收完全),可以测定其中H2以及 CO 的物质的量。

可供选用的装置如下所示(省略夹持仪器):
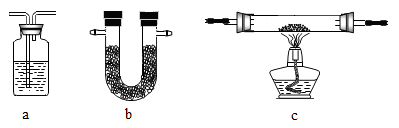
为装置Ⅰ~Ⅴ选择合适的装置与试剂:
装置Ⅰ、Ⅱ的作用是____________ 。要确定半水煤气中H2物质的量,应测量的数据是______ 。

(1)在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应实现了 CO 变换,其化学方程式为:
(2)吸收法是脱除CO2的方法之一。已知:
| 溶质 | Na2CO3 | K2CO3 |
| 20℃1L饱和溶液中溶质的物质的量mol | 2.0 | 8.0 |
| 溶质价格(元/kg) | 1.25 | 9.80 |
若选择Na2CO3溶液作吸收液,其优点是
(3)将一定体积半水煤气依次通过装置Ⅰ~Ⅴ(最后通入氮气确保反应、吸收完全),可以测定其中H2以及 CO 的物质的量。

可供选用的装置如下所示(省略夹持仪器):

为装置Ⅰ~Ⅴ选择合适的装置与试剂:
| 装置 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| a | a | b | |||
| 试剂 | 浓硫酸 | CuO |
装置Ⅰ、Ⅱ的作用是
26.为探究某物质 X 对钢铁在潮湿环境下的腐蚀的影响作用,某同学进行了如下实验:
① 选择 6 个容量相同的烧瓶,分别编号为 1~6,加入规格、质量相同的铁丝。
② 向 1~3 号瓶中放入 2mL 清水,向 4~6 号瓶中放入 2mL10%X 的水溶液,将铁丝润湿。
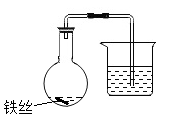
③ 塞上带有导管的塞子,将导管末端浸入盛有水的烧杯中,记录导管内液面的初始位置(如图所示)。
④ 放在室温环境下,每隔一小时测量一次,周期为 3 小时,记录数据。结果如下表所示:
注:放置过程中导管内液面上升情况(单位:cm)
(1)在该项探究中,要取同样处置的 3 只烧瓶的目的是_ 。
(2)6 号瓶的数据明显与 4、5 号瓶不同,可能原因是_ 。
(3)通过本实验,可初步得出的结论是_ 。
(4)该项探究的设计是否存在不足_ ?如何改进_ ?

① 选择 6 个容量相同的烧瓶,分别编号为 1~6,加入规格、质量相同的铁丝。
② 向 1~3 号瓶中放入 2mL 清水,向 4~6 号瓶中放入 2mL10%X 的水溶液,将铁丝润湿。
③ 塞上带有导管的塞子,将导管末端浸入盛有水的烧杯中,记录导管内液面的初始位置(如图所示)。
④ 放在室温环境下,每隔一小时测量一次,周期为 3 小时,记录数据。结果如下表所示:
| 时间(小时) | 1 号瓶 | 2 号瓶 | 3 号瓶 | 4 号瓶 | 5 号瓶 | 6 号瓶 |
| 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| 1 | 0 | 0.1 | 0 | 1.2 | 1.4 | 0 |
| 2 | 0.8 | 0.7 | 0.9 | 5.6 | 5.7 | 0.1 |
| 3 | 3.5 | 3.2 | 3.7 | 9.8 | 10.0 | 0.1 |
注:放置过程中导管内液面上升情况(单位:cm)
(1)在该项探究中,要取同样处置的 3 只烧瓶的目的是
(2)6 号瓶的数据明显与 4、5 号瓶不同,可能原因是
(3)通过本实验,可初步得出的结论是
(4)该项探究的设计是否存在不足
27.某工业生产流程如图所示:
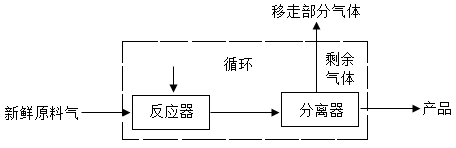
每生成1t 产品,需要通入含有0.2%(体积分数,下同)的惰性杂质CH4的新鲜原料气2800m3。
经分离器分离产品后,剩余气体中含有大量未充分反应的原料与 3%的CH4。在连续生产的条件下,可对剩余气体采用部分循环、部分移走的操作,一方面能提高原料的利用率,节省成本,另一方面也避免装置中CH4越来越多而对生产造成不利影响。已知在此生产条件下,CH4在每吨产品中的溶解量为2.3m3,。计算每生产 1t 产品需要移走气体的体积。

每生成1t 产品,需要通入含有0.2%(体积分数,下同)的惰性杂质CH4的新鲜原料气2800m3。
经分离器分离产品后,剩余气体中含有大量未充分反应的原料与 3%的CH4。在连续生产的条件下,可对剩余气体采用部分循环、部分移走的操作,一方面能提高原料的利用率,节省成本,另一方面也避免装置中CH4越来越多而对生产造成不利影响。已知在此生产条件下,CH4在每吨产品中的溶解量为2.3m3,。计算每生产 1t 产品需要移走气体的体积。
28.实验室有一包食盐,已经过初步提纯,除去了难溶性杂质,但仍含有CaSO4、MgSO4、CaCl2、MgCl2杂质。现取该食盐样品20.000g,测得其中含有Ca、Mg两种元素共0.300g,S元素0.064g(其他杂质忽略不计)。
(1)该食盐中CaSO4与MgSO4的物质的量之和为mol。
(2)计算该食盐中NaCl的质量分数的范围。
(1)该食盐中CaSO4与MgSO4的物质的量之和为mol。
(2)计算该食盐中NaCl的质量分数的范围。
 搜索
搜索
 难度系数:0.85
难度系数:0.85  答案解析
答案解析
 有奖纠错
有奖纠错
