全一卷
1.每年的3月22日是“世界水日”,“国家节水标志”的图标是
A. | B. | C. | D. |
2.下列变化属于化学变化的是
| A.石蜡熔化 | B.谷物酿酒 |
| C.蔗糖溶解 | D.酒精挥发 |
3.下列物质属于酸的是
| A.P2O5 | B.NaHCO3 |
| C.NH3﹒H2O | D.CH3COOH |
4.下列说法中错误的是
| A.空气是混合物 |
| B.空气中氧气与氮气体积比约为4:1 |
| C.氧气不易溶于水 |
| D.医疗上可在液氮冷冻麻醉条件下做手术 |
5.页岩气是指蕴藏于页岩层中的天然气,是一种新开发的能源。下列说法错误的是
| A.页岩气的主要成分是甲烷 |
| B.页岩气是不可再生能源 |
C.其完全燃烧的化学方程式为: |
| D.页岩气燃烧放出热量 |
6.下列实验操作错误的是
A.仪器连接 | B.滴加液体 |
C.振荡试管 | D.倾倒液体 |
7.我国《新型冠状病毒感染的肺炎诊疗方案(试行第三版)》中提到可试用利托那韦进行抗病毒治疗,利托那韦的化学式为C37H48N6O5S2,下列关于利托那韦分子说法中正确的是
| A.由5种元素组成的混合物 |
| B.每个分子中含2个硫元素 |
| C.氮、氧原子个数比为6:5 |
| D.氢元素的质量分数最高 |
8.下列物质中碱性最强的是
| 物质 | 液体肥皂 | 西瓜汁 | 胆汁 | 牛奶 |
| pH | 9.5~10.5 | 5.3~6.2 | 7.1~7.3 | 6.3-6.6 |
| A.液体肥皂 | B.西瓜汁 | C.胆汁 | D.牛奶 |
9.下列说法错误的是
| A.葡萄糖是有机高分子化合物 |
| B.多吃果蔬可以补充维生素 |
| C.炒菜用加碘盐可补充碘元素 |
| D.生活中常用煮沸的方法软化硬水 |
10.“84消毒液”的有效成分次氯酸钠(NaClO)中,氯元素的化合价为
| A.-1 | B.+1 | C.+5 | D.+7 |
11.稀土有“工业的维生素”的美誉。稀土元素铥的信息如图所示,下列说法错误的是
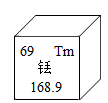

| A.该元素的元素符号为Tm |
| B.该元素是金属元素 |
| C.该元素原子的质子数为69 |
| D.该元素原子的相对原子质量为168.9克 |
12.下列说法正确的是
| A.水由氢气和氧气组成 |
| B.电解水实验中,正极与负极产生的气体体积比约为2:1 |
| C.用水灭火的原理是降低可燃物的着火点 |
| D.明矾、活性炭都可用于水的净化 |
13.下列现象描述错误的是
| A.打开盛有浓盐酸的试剂瓶瓶盖,出现白雾 |
| B.CO2通入紫色石蕊溶液,溶液变蓝 |
| C.将浓硫酸滴到白纸上,白纸变黑 |
| D.铁丝在氧气中剧烈燃烧,火星四射,产生黑色固体 |
14.下列化学方程式书写正确的是
A.硫在氧气中燃烧: |
B.CO2使澄清石灰水变浑浊: |
C.Ba(OH)2溶液与Na2SO4溶液混合: |
D.一氧化碳从氧化铁中还原出铁: |
15.甲、乙、丙、丁四种物质在反应前后的质量关系如图表示,下列说法错误的是


| A.该反应是化合反应 |
| B.甲可能是化合物 |
| C.丙一定是该反应的催化剂 |
| D.反应前后乙和丁变化的质量比为8:15 |
16.化学用语是学习化学的重要工具,请用化学用语填空。
(1)2个氢原子____________。
(2)硝酸根离子___________。
(3)高锰酸钾____________。
(4)写出氢氧化镁的化学式并标出镁的化合价_________。
(1)2个氢原子____________。
(2)硝酸根离子___________。
(3)高锰酸钾____________。
(4)写出氢氧化镁的化学式并标出镁的化合价_________。
17.化学知识与我们的生产生活密切相关,请从下列物质中选择填空(填字母)。
(1)属于合金的是________。
(2)属于复合肥的是________。
(3)可形成酸雨的是__________。
(4)可用于制铅笔芯的是__________。
| A.石墨 | B.磷铵 | C.不锈钢 | D.二氧化硫 |
(2)属于复合肥的是________。
(3)可形成酸雨的是__________。
(4)可用于制铅笔芯的是__________。
18.下表是元素周期表的一部分,回答问题:
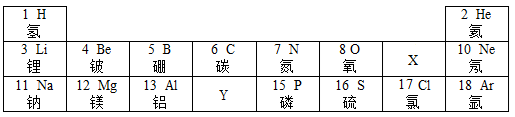
(1)写出X的元素符号_______。
(2)画出元素Y的原子结构示意图_________。
(3)13号元素和17号元素形成的化合物的化学式为_________。
(4)16号元素的原子在化学反应时容易_______(填“得到”或“失去”)电子,形成的简单离子表示为________。

(1)写出X的元素符号_______。
(2)画出元素Y的原子结构示意图_________。
(3)13号元素和17号元素形成的化合物的化学式为_________。
(4)16号元素的原子在化学反应时容易_______(填“得到”或“失去”)电子,形成的简单离子表示为________。
19.甲、乙两种物质的溶解度曲线如图。

(1)A点的含义是___________。
(2)t2℃时,甲、乙两种固体各8g分别投入25g水中,充分搅拌。
①________(填“甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入溶质_____g可使其达到饱和。
②乙所得溶液中溶质质量分数为_____%。

(1)A点的含义是___________。
(2)t2℃时,甲、乙两种固体各8g分别投入25g水中,充分搅拌。
①________(填“甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入溶质_____g可使其达到饱和。
②乙所得溶液中溶质质量分数为_____%。
20.2022年第24届冬季奥运会将在北京市和张家口市联合举行。如图所示,“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是HCl、CuO、H2、CuSO4中的一种。

(1)写出下列物质的化学式:A_______ ,D _______ 。
(2)写出B与C发生反应的化学方程式:______________ 。

(1)写出下列物质的化学式:A
(2)写出B与C发生反应的化学方程式:
21.“粗盐中难溶性杂质的去除”实验操作的主要步骤如图。
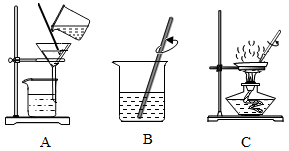
(1)操作A的名称为______ 。
(2)操作C中玻璃棒的作用是_________ 。
(3)正确的操作顺序为_____________ (填字母)。

(1)操作A的名称为
(2)操作C中玻璃棒的作用是
(3)正确的操作顺序为
22.根据下列实验装置图,回答有关问题。
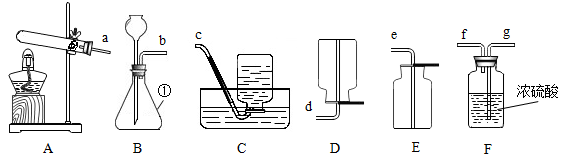
(1)图中标有①的仪器名称为_______ 。
(2)实验室用加热熟石灰与氯化铵固体的方法可以制取氨气,其发生装置选用_________ (填大写字母)。
(3)实验室用锌粒和稀硫酸制取H2的发生装置选用____________ (填大写字母),反应的化学方程式为______________ 。
(4)实验室用双氧水和二氧化锰制取一瓶干燥的氧气,所选仪器的接口连接顺序是______________ 填导管接口的小写字母)。

(1)图中标有①的仪器名称为
(2)实验室用加热熟石灰与氯化铵固体的方法可以制取氨气,其发生装置选用
(3)实验室用锌粒和稀硫酸制取H2的发生装置选用
(4)实验室用双氧水和二氧化锰制取一瓶干燥的氧气,所选仪器的接口连接顺序是
23.某实验小组将少量氢化钙(CaH2)溶于水,形成了无色透明的溶液,再向其中加入碳酸钠溶液,有沉淀产生,经过滤后得到滤渣和滤液。然后进行了滤渣验证和滤液溶质成分的探究。
(1)【查阅资料】氢化钙在常温下能与水反应生成氢氧化钙和氢气,写出该反应的化学方程式______________ 。
(2)【交流验证】滤渣只能是碳酸钙,用盐酸验证此滤渣的化学方程式为______________ 。
(3)【提出问题】滤液中溶质的成分是什么?
(4)【猜想假设】猜想一:NaOH
猜想二:NaOH和Na2CO3
猜想三:NaOH和________ 。
猜想四:NaOH、Na2CO3和Ca(OH)2
(5)【讨论分析】经过讨论认为最不合理的是猜想____ ,原因是______________ 。
(6)【实验与结论】
(7)【拓展延伸】在分析反应后所得物质的成分时,除考虑生成物外,还需考虑___________ 。
(1)【查阅资料】氢化钙在常温下能与水反应生成氢氧化钙和氢气,写出该反应的化学方程式
(2)【交流验证】滤渣只能是碳酸钙,用盐酸验证此滤渣的化学方程式为
(3)【提出问题】滤液中溶质的成分是什么?
(4)【猜想假设】猜想一:NaOH
猜想二:NaOH和Na2CO3
猜想三:NaOH和
猜想四:NaOH、Na2CO3和Ca(OH)2
(5)【讨论分析】经过讨论认为最不合理的是猜想
(6)【实验与结论】
| 实验步骤 | 现象 | 结论 |
| 步骤I:取少量滤液,向其中加入足量盐酸溶液 | 猜想二不成立 | |
| 步骤Ⅱ:另取少量滤液,向其中滴入适量Na2CO3溶液 | 产生白色沉淀 | 猜想 |
(7)【拓展延伸】在分析反应后所得物质的成分时,除考虑生成物外,还需考虑
24.取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图。
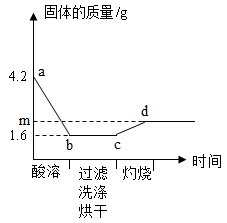
(1)b点时溶液中溶质的化学式为 。
(2)原粉状混合物中铁粉的质量为多少克。
(3)求m的值。(写出计算过程)

(1)b点时溶液中溶质的化学式为 。
(2)原粉状混合物中铁粉的质量为多少克。
(3)求m的值。(写出计算过程)
 搜索
搜索
 难度系数:0.94
难度系数:0.94  答案解析
答案解析
 有奖纠错
有奖纠错
